yogabuch / bewegungsphysiologie / nervensystem
Siehe auch die Seite mit Karten zu Nerven
Inhaltsverzeichnis
- 1 Nervensystem
- 2 Nerv
- 3 Einteilungen des Nervensystems
- 4 Begriffe und Teile des Nervensystems
- 5 Einige Begriffe
- 5.1 Allodynie
- 5.2 exzitatorisch
- 5.3 Hyperalgesie
- 5.4 Hyperpathie
- 5.5 inhibitorisch
- 5.6 Kausalgie
- 5.7 Parästhesie
- 5.8 Hypästhesie
- 5.9 Blut-Hirn-Schranke
- 5.10 Cauda equina
- 5.11 Dermatom
- 5.12 Golgi-Sehnenorgan
- 5.13 Hirnhäute
- 5.14 Hirnnerven
- 5.15 Medulla oblongata
- 5.16 Intramuskuläre Koordination
- 5.17 Ischiasnerv
- 5.18 Kennmuskeln
- 5.19 Motoneuronen
- 5.20 Myotom
- 5.21 Nervenkompressions-Syndrom
- 5.22 Nervenwurzel
- 5.23 Nervenwurzelkompressions-Syndrom
- 5.24 neuroradikulär
- 5.25 Plexus brachialis
- 5.26 Plexus lumbosacralis
- 5.27 Plexus lumbalis
- 5.28 Plexus sacralis
- 5.29 Propriozeption
- 5.30 Propriozeptoren
- 5.31 Pyramidenbahn (Tractus pyramidalis)
- 5.32 Pyramidenbahnzeichen
- 5.33 Rückenmark
- 5.34 Spinalkanal
- 5.35 Spinalnerv
- 5.36 Liquor
- 5.37 Parasympathikoton
- 5.38 Sympathikoton
- 5.39 Vagusnerv (N. vagus)
- 5.40 vagoton
- 6 Schmerz
- 7 Hysterical Strength Pathway
- 8 Schmerzanamnese (Kurzform)
- 9 Charakteristische Schmerzen
- 9.1 Anlaufschmerz (Einlaufschmerz, Loslaufschmerz)
- 9.2 Belastungsschmerz (stress induced pain)
- 9.3 Belastungsschmerzhaftigkeit
- 9.4 Bewegungsschmerz (pain in motion)
- 9.5 Bewegungsschmerzhaftigkeit
- 9.6 Dehnungsschmerz
- 9.7 Dehnungsschmerzhaftigkeit
- 9.8 Druckschmerz
- 9.9 Druckschmerzhaftigkeit / Druckdolenz
- 9.10 funktioneller Schmerz
- 9.11 ischämischer Schmerz (Ischämieschmerz, ischemic pain)
- 9.12 Klopfschmerz
- 9.13 Leistenschmerz
- 9.14 Nachbelastungsschmerz (Schmerznachhall)
- 9.15 Nachtschmerz
- 9.16 Pseudoradikulärer Schmerz
- 9.17 pulssynchroner Schmerz (Pochen, Klopfen)
- 9.18 Radikulärer Schmerz
- 9.19 Ruheschmerz
- 9.20 Spannungsschmerz
- 9.21 Struktureller Schmerz
- 9.22 Wachstumsschmerz
Nervensystem
Ein Nervensystem besteht aus Nervenzellen (Neuronen) und stützenden und isolierenden Gliazellen. Es muß nicht unbedingt, wie beim Menschen ein Gehirn besitzen. Aufgabe des NS ist es, Veränderungen in der Außen- und Innenwelt zu registrieren, aufeinander zu beziehen und mit früheren zu vergleichen, um daraus ggf. Reaktionen zu veranlassen.
Die einfachste Form ist ein diffuses Nervensystem oder Nervennetz aus vielen einzelnen Nervenzellen (Neuronen) ohne Koordinationszentren zur zentralen Steuerung. Erregungen werden dabei teilweise in beide Richtung eines Nervs geleitet. Im Laufe der Höherentwicklung der Wesen kommen Ganglien (Nervenknoten im PNS, bei Säugetieren sind anderthalb Dutzend verschiedener Typen bekannt) dazu, die sich in sensible und autonome Ganglien gliedern lassen. und später Gehirne. Alle Wirbeltiere besitzen ein Gehirn und ein durch die Wirbel verlaufendes Rückenmark, die zusammen das Zentrale Nervensystem ZNS bilden. Der Rest des NS wird als PNS bezeichnet, dortige Nerven brauchen eine Bindegewebshülle. Das menschliche Gehirn ist nicht nur DAS Nervenzentrum des Körpers sondern besitzt mit dem Hypothalamus (unter dem Thalamus liegend) auch eine der wichtigsten Drüsen von global steuernder Bedeutung.
Nervenimpuls
Nervenimpulse dienen der sehr kurzfristigen Steuerung. Unmyelinisierte (marklose, „unisolierte“) Nervenfasern leiten nur mit einer Geschwindigkeit von etwa 1m/s (3,6 km/h), dicke myelinisierte Fasern können bis 100m/s (360 km/h) schnell leiten. Generell wird über alle Säugetiere eine Geschwindigkeit von 0,2 bis 120 m/s angenommen. Dagegen setzt die Wirkung von Hormonen über den Blutstrom langsamer ein. In den schnellsten Blutgefäßen wie etwa der Halsschlagader liegt die Geschwindigkeit bei etwa 1 m/s und damit auf dem Niveau der langsamsten Nerven. In den kleinen Geweben der Schilddrüse etwa fließt das Blut nur noch mit 3-5 cm/s, also gerade einmal rund 0,15 km/h.
Nervenfaser
Eine Nervenfaser ist der langgestreckte Fortsatz einer Nervenzelle und seiner aus Gliazellen gebildeten Umhüllung. Fortsatz mit Hülle werden auch als Axon bezeichet. Dickere Axone leiten schneller als dünnere. Wirbeltiere wie der Mensch können Axone mit mehreren Lagen isolierender Gliazellen haben, die besonders schnell leiten, diese Umhüllung heißt Myelinscheide. Die hohe Nervenleitgeschwindigkeit ist eine Notwendigkeit für schnelle Bewegungen großer Körper wegen deren langen Nervenbahnen. Kalmare, deren Bewegungsapparat ohne Myelinscheiden auskommt, brauchen 100 mal dickere Nerven mit Riesenaxonen, die nur etwa 60 m/s Leitgeschwindigkeit erreichen. Die Nervenlaufzeit ist nicht temperaturunabhängig, die Geschwindigkeit steigt (im physiologischen Bereich) um 1-2 m/s pro Grad. Myelinisiert sind meist solche Nervenfasern, die sensorische oder motorische Reize über längere Strecken übertragen und etwas mit dem Verhältnis des Menschen zu seiner Außenwelt zu tun haben.
Nerv
Als Nerv bezeichnet man eine Vielzahl von durch zusätzliche bindegewebige Hüllen ummantelte Nervenfasern. Innervation ist die Versorgung von Organen oder Körperteilen durch Nervenfasern und deren Reizübertragung. Man unterscheidet
– afferente (zum ZNS führende) und efferente (vom ZNS weg führende) Nervenfasern. Weiter wird
– nach Art der Myelinisierung und damit Nervenleitgeschwindigkeit unterschieden sowie
– nach Wirkung: sensibel (Wahrnehmung), motorisch (Bewegungsapparat), vegetativ (autonomes NS mit den Teilen sympathisch, parasympathisch und enterisch).
Sensibles und motorisches NS werden zusammen auch als somatisches NS bezeichnet (äußere Wahrnehmnug und Motorik). Das sympathische NS ist ergotrop, steigert also die nach außen gerichtete Handlungsfähigkeit bei tatsächlicher oder gefühlter Belastung (fight or flight). Das parasympathische NS ist trophotrop, dient also dem Aufbau körpereigener Reserven in Ruhe und Erholung (rest and digest). Das enterische NS kann völlig autonom die Funktion der Verdauungsorgane regeln, wird aber durch Sympathikus und Parasympathikus beeinflußt, die deren Funktion in den aktuellen Kontext des Gesamtsystems stellen. Es durchzieht fast den gesamten Magen-Darm-Trakt. Beim Menschen besitzt es fünfmal mehr Neuronen als das Rückenmark.
motorische Endplatte
Eine motorische Endplatte ist eine Synapse, an der eine Motorische Nervenfaser ihr Potential chemisch mittels Neurotransmitter Acetylcholin, auf eine Muskelfaser überträgt. Das Acetylcholin wird vom präsynaptischen Anteil des Sarkolemms der Nervenzelle über den synaptischen Spalt auf den postsynaptischen Anteil des Sarkolemms einer Muskelfaser übertragen. Die motorische Endplatte besteht aus dem Endknöpfchen (präsynaptische Endigung), dem synaptischen Spalt von 10-15 µm Breite und dem Membranabschnitt der Muskelzelle. Sowohl dieser Membranabschnitt als auch das Endknöpfchen sind stark aufgefaltet und verhalten sich komplementär. Die Aktionspotentiale des Axons bewirken die Öffnung von spannungsgesteuerten Ca-Kanälen, und das freigesetzte Ca mobilisiert synaptische Vesikel, die den Neurotransmitter Acetylcholin enthalten, der dann in den synatischen Spalt emittiert wird und von Rezeptoren der postsynaptischen Membran aufgenommen wird. Während die Verteilung im Spalt per Diffusion geschieht, verbraucht allein schon der Vesikeltransport im Endköpfchen der Nervenzelle Energie. Die Bindung des Acetylcholins an die entsprechenden Rezeptoren führt zur Öffnung von (Kat-)Ionenkanälen in der Muskelzelle, was einen Stromfluß bewirkt, der letzlich in der Muskelzelle über die breitflächige Freisetzung von Calciumionen, die jedes Sarkomer der Myofibrille erreichen, zu der Freigabe von Bindungsstellen für das Motorprotein Myosin an den Aktinfilamenten und damit zur Kontraktion der Muskelzelle führt. Das im Gelenkspalt nicht verwendete Acetylcholin wird von dem Enzym Acetylcholinesterase zerlegt und der Cholin-Anteil von der präsynaptischen Membran wiederaufgekommen und recycelt. Nach der Zerlegung ist ist es an der postsynaptischen Membran wirkungslos. Das Cholin kann von der präsynaptischen Membran durch den Cholin-Reuptake-Transporter wiederverwendet werden. Eine Störung der Acetylcholinrezeptoren, etwa durch Autoantikörper führt zu Störungen wie der Myasthenia gravis.
Mit wenigen Ausnahmen werden die Muskeln des Bewegungsapparates nicht direkt vom Gehirn gesteuert sondern über zwei Motoneuronen, das UMN und das LMN, auch als 1. Motoneuron und 2. Motoneuron bezeichnet.
Die Übertragung von Nervenimpulsen beruht auf Aktionspotentialen. Als solche werden vorübergehende Abweichungen des Potentials der Zellmembran von ihrem Ruhepotential bezeichnet. Nerven- und Muskelzellen können Aktionspotentiale bilden und diese Erregung leiten. Die Übertragung zwischen Nervenzellen geschieht meist durch Neurotransmitter, wie auch von Nerven zu Muskelzellen. Neben erregenden Potentialen sind damit auch hemmende Potentiale möglich. Muskelzellen interagieren nicht selten direkt elektrisch.
motorische Einheit
Eine motorische Einheit ist ein die Gesamtheit eines Motoneurons mit den von diesem innervierten Muskelfasern und damit die kleinste funktionelle Einheit willkürlicher und unwillkürlicher Motorik. Die kleinsten motorischen Einheit beim Menschen besitzen 100-300 Muskelfasern (Muskeln des Auges und der Finger), die größten bis 2000 (Quadrizeps). Dabei ensprechen sich weitgehend die Größe des Zellkerns des Motoneurons, Dicke des Axons und die Anzahl der Muskelfasern. Die Muskelfasern einer Motorischen Einheit liegen nicht nebeneinander, sondern sind über den Muskel auf einem Querschnitt von etwa 1 cm² verteilt. Für geringe Kraftausübung wie Feinmechanik werden kleine Motorische Einheiten rekrutiert, für größere Kräfte große Motorische Einheiten. Für eine maximale Kraftausübung wird die neuronale Impulsfrequenz der aquirierten Motorischen Einheiten gesteigert, so daß sich die einzelnen Zuckungen der Muskelfasern überlagern und die resultierende Kraft summiert.
neuroendokrines System
Lange Zeit ging man davon aus, daß das Nervensystem mit
Neurotransmittern und Gap junctions arbeite, während das Endokrinium ein davon weitgehend getrenntes System sei, welches Hormone ins Blut sezerniert. Die Tatsache, daß Neuronen nicht nur Neurotransmitter bilden und freisetzen, sondern auch Hormone freisetzen können, und auf der anderen Seite Neurotransmitter hormonbildende Zellen aktivieren, legt eine allgemeinere Sichtweise nahe und führt zu dem Begriff des neuroendokrinen Systems. Das sind alle anatomischen Strukturen (Zellen, Organe, Gewebe von Organen), die Neurohormone prozessieren oder sezernieren. Beim Menschen ist das Hypothalamus-Hypophysen-System ein neuroendokrines System mit der Neurohypophyse als Neurohämalorgan, in das der Hypothalamus mit den Axonen seiner neurosekretorischen Neuronen Hormone abgibt. Zum neuroendokrinen System des Menschen gehören Hypothalamus-Hypophysen-System Epiphyse Nebenschilddrüse Nebennierenmark Pankreasinseln C-Zellen der Schilddrüse Paraganglien Das Diffuse NeuroEndokrine System (DNES, auch AUPD-System, Amine Precursor Uptake and Decarboxylation) mit verschiedenen Zellen im GIT, Pankreas, UGT, Bronchialsystem und weiteren Organen. Während höhere Tiere das Hypothalamus-Hypophysen-System besitzen, gibt es etwa bei Insekten ein anderes Neurohämalorgan.
Einteilungen des Nervensystems
Das Nervensystem kann auf verschiedene Weise eingeteilt werden:
nach Lage: peripheres und zentrales Nervensysstem
Peripheres Nervensystem (PNS)
der Teil des Nervensystems, der nicht zum ZNS gehört, also nicht von Knochen umgeben sind.
Zentrales Nervensystem (ZNS)
der Teil des Nervensystems, der von Knochen umgeben ist, also Gehirn und der Teil der Spinalnerven, der im Rückenmarkskanal verläuft. Nach dem Austritt über die Zwischenwirbellöcher zählen die entsprechenden Anteile der Spinalnerven wie auch alle peripheren nerven zum PNS.
nach willkürlicher/unwillkürlicher Steuerung (somatisch/autonom)
Somatisches Nervensystem / wilkürliches Nervensystem / animalisches Nervensystem / cerebrospinales Nervensystem
Das Somatische Nervensystem ist der Teil des Nervensystems, der eine bewußte Steuerung des Körpers über die Muskeln (Willkürmotorik) ermöglicht und seine bewußte Sensorik beinhaltet, sowohl für den eigenen Körper als auch für die Umwelt. Es enthält also sowohl einen afferenten als auch einen efferenten Anteil. Die Afferenzen bilden die aufsteigenden Projektionsbahnen und führen zu den Projektionszentren und damit mittelbar auch zu den Assoziationszentren. Zu den
Afferenzen gehören insbesondere die Nerven der Sinne. Die Efferenzen versorgen ausschließlich quergestreifte Muskulatur, darunter die motorischen Anteile der Hirnnerven (z.B. Augenbewegung und Gesichtsmimik) und über die Pyramidenbahnen (PS, pyramidales System, auch: Tractus corticospinalis) die ganze übrige Skelettmuskulatur. Ein weiterer Anteil, das extrapyramidale System (EPS) führt weitgehend automatisierte Bewegungsmuster aus, die es aus den vielfach wiederholten Mustern des PS übernimmt. Die pyramidal angesteuerten Muskeln haben zwei serielle Motoneuronen, die von den
Hirnnerven gesteuerten eins: das Upper Motoneuron (UMN) und das
Lower Mononeuron (LMN). Die Zellkörper (Betzsche Riesenzellen) des
UMN befinden sich in der motorischen Rinde im Gehirn, die zugehörigen
Axone in der Pyramidenbahn. Die UMN steuern nie direkt die Muskeln an, sondern immer über die LMN. Die Zellkörper der LMN liegen im Vorderhorn der grauen Substanz des Rückenmarks und bilden im gesamten Rückenmark die motorische Kernsäule. In jedem Wirbelsegment treten Axone als Teil der Spinalnerven aus und von dort sich verästelnd zu den motorischen Endplatten der Muskeln des zugehörigen Myotoms.
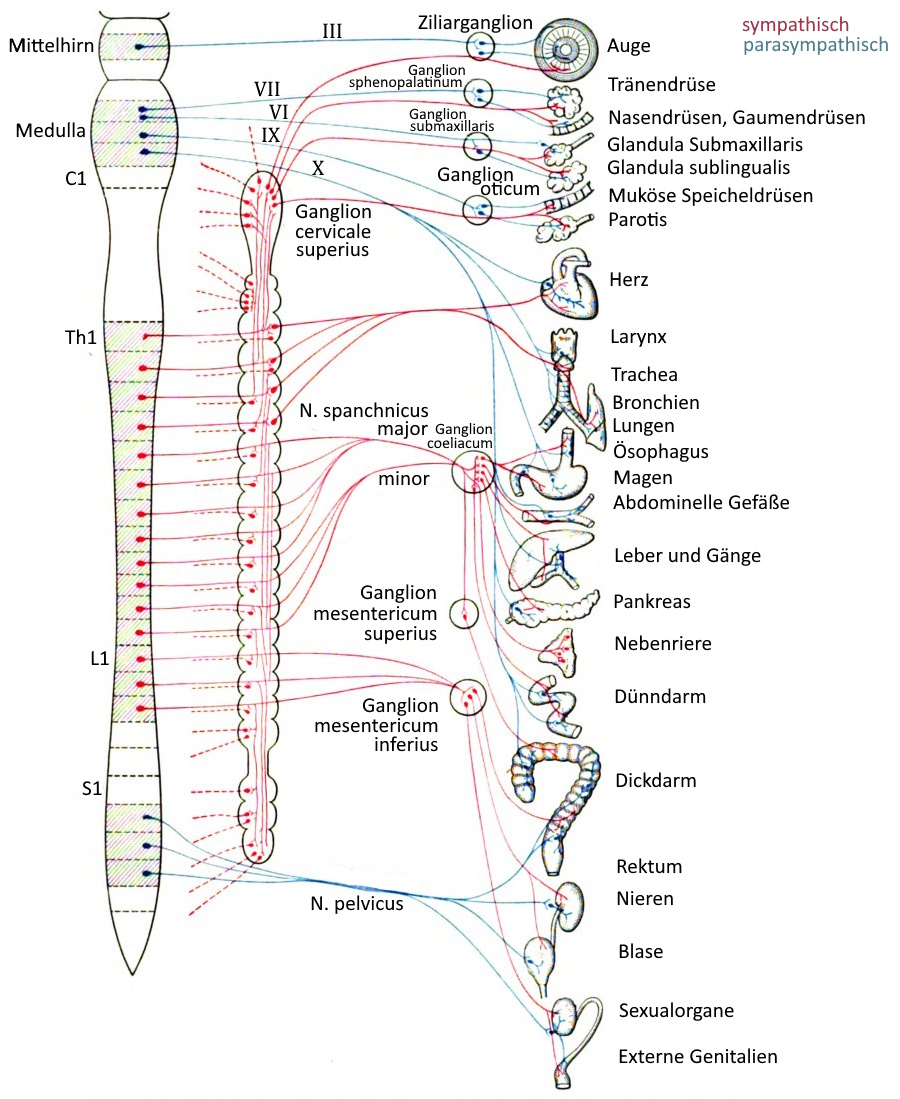
Vegetatives Nervensystem
Das vegetative Nervensystem ist der unwillkürlich den Körper steuernde Teil des Nervensystems. Es enthält sowohl einen afferenten als auch einen efferenten Anteil. Eine direkte, willentliche Steuerung ist nicht möglich, bestenfalls mittelbare Einflußnahme. Atmung, Verdauung, Stoffwechseln und Herzschlag unterliegen dem Autonomen Nervensystem, wobei die Lunge ein Beispiel dafür ist, daß Organe von beiden Teilen des Nervensystems beeinflußt werden können. Auch die Sexualorgane, endokrine und exokrine Drüsen und das Blutgefäßsystem unterliegen teils oder gänzlich dem Autonomen Nervensystem. Es kann unterteilt werden in:
- Sympathisches Nervensystem / Sympathikus Parasympathisches
- Nervensystem / Parasympathikus, darunter ist der
N. vagus von herausragender Bedeutung
Das enterisches Nervensystem ist ein selbständiges Regelsystem des Verdauungstrakts, das aber auf Signale des Sympathikus oder N. vagus reagiert. Der ergotrope Sympathikus und der trophotrope Parasympathikus agieren teils antagonistisch, teils synergistisch. Die wichtigsten Regulationszentren des Autonomen Nervensystems liegen im Hirnstamm und im Hypothalamus, die diverse Regelkreise etablieren. Körperliche Tätigkeit, aber in Abschwächung auch schon die Vorstellung davon beeinflußt als willkürliche Tätigkeit mit Ausmaß und Art das Autonome Nervensystem mittelbar. Efferente motorische Nervenfasern des vegetativen Nervensystems innervieren mit Ausnahme des Einflusses auf Skelettmuskeln nur glatte Muskulatur. Das Verdauungssystem ist das größte vegetative Organsystem. Das begriffliche Gegenstück zum autonomen (vegetativen) Nervensystem ist das somatische/animalische Nervensystem, welches eine bewußte Steuerung des Körpers ermöglicht und seine bewußte Sensorik beinhaltet. Beide Teile des Nervensystems sind in ZNS und PNS repräsentiert.
nach Ausrichtung der Leitung: afferent/efferent
afferente Nerven / Afferenz
afferente Nerven sind solche, die sensorische Reize (Sinnesorgane, aber auch Propriozeption) zum ZNS (Gehirn und Rückenmark) leiten.
Auf ein Neuron selbst bezogen sind die Dendriten afferent und die Neuriten efferent.
efferente Nerven / Efferenz
efferente Nerven sind solche, die Informationen aus dem ZNS in die Peripherie (Nerven, Organe) leiten, insbesondere versteht man unter efferenten Fasern die Axone der Neuronen.
Auf ein Neuron selbst bezogen sind die Dendriten afferent und die Neuriten efferent.
nach grobem Einfluß auf den Körper: sympathisch/parasympathisch
Sympathikus
Der Sympathikus ist der Teil des vegetativen Nervensystems, der die Leistungssteigerung und Mobilisierung von Energiereserven steuert. Diese Wirkungen werden als ergotrop bezeichnet. Er ist dabei weitgehend antagonistisch zum Parasympathikus. Der Sympathikus ist am Herzen positiv chronotrop, positiv dromotrop (Reizleitung beschleunigend), positiv inotrop (Kontraktionskraft verstärkend), positiv bathmotrop (Reizschwelle senkend), positiv lutitrop (Erschlaffung fördernd) und steigert damit das Herzzeitvolumen auf jede mögliche Weise. In den Blutgefäßen wirkt er vasokonstriktiv, auf die Bronchien dilatierend und Schleimproduktion hemmend und schleimverflüssigend, im Gastrointestinaltrakt vermindert er Drüsensekretion und Peristaktik, im UGT strafft er den Blasensphinkter und schwächt den Musculus detrusor vesicae, im Auge bewirkt er eine Mydriasis (Weitstellung der Pupille) und führt allgemein zu verermehrter Schweißsekretion. Eine erhöhte Erregung des Sympatikus wird als Sympathikotonus bezeichnet, er wirkt HRV abschwächend.
Parasympathikus
Der Parasympathikus ist der Teil des vegetativen Nervensystems, das für Regeneration und Aufbau von Energiereserven zuständig ist und damit weitgehender Gegenspieler zum ergotropen Sympathikus, der Leistungssteigerung und Mobilisierung von Energiereserven steuert. Diese Wirkungen des Sympathikus werden als ergotrop bezeichnet. Er ist damit weitgehend antagonistisch zum Parasympathikus. Zu den Nervenfasern des Parasympathikus gehören einige der Hirnnerven III (Nervus oculomotorius), VII (Nervus facialis), IX (Nervus glossopharyngeus) und besonders X (N. vagus). Auch der Trigeminus führt streckenweise parasympathische Fasern, die jedoch vom N. facialis stammen. Der Parasympathikus wirkt am Herzen negativ chronotrop und negativ dromotrop (Erregungsleitung fördernd), im Genitalbereich auf die Gefäße vasodilatorisch, in den Bronchien konstriktiv und schleimsekretionsfördernd, verstärkt im Verdauungstrakt Sekretion und Peristaltik, ist im UGT miktionsfördernd, fördert die Kontraktion des Uterus, fördert Miosis (Pupillenengstellung) und Akkomodation und fördert die Speichelproduktion. Eine erhöhte Erregung des Parasympatikus wird als Parasympathikotonus oder meist als Vagotonus bezeichnet, er wirkt HRV verstärkend.
Begriffe und Teile des Nervensystems
Reflexe
Ein Reflex ist eine neuronal vermittelte unwillkürliche, rasche, gleichartige Reaktion eines Organismus auf einen bestimmten Reiz. Der einfachste Fall ist der einfache monosynaptische Reflexbogen (Eigenreflex: Rezeptor und Effektor liegen im selben Organ), bei dem ein Rezeptor (afferent, Sinneszelle) mit dem Effektor (efferent, z.B. Muskel, Drüse) direkt über eine Synapse im Vorderhorn des Rückenmarks verschaltet ist. Beispiele für einen Eigenreflex sind Patellarsehnenreflex und Achillessehnenreflex. Dabei sind die Begriffe irreführend, weil der reflexauslösende Rezeptor nicht in der Sehne sondern im Muskel liegt, es müßte also heißen Quadrizepsreflex und Triceps-Surae-Reflex. Bei polysynaptischen Reflexen liegen Rezeptor und Effektor meist räumlich getrennt, weshalb sie auch als Fremdreflexe bezeichnet werden. Beispiel: Der durch einen Fremdkörper im Hals (Drucksensoren) ausgelöste Hustenreiz, der die exspiratorische Muskulatur (Effektor) innerviert. Reflexbögen sind die einfachsten Sonderfälle neuronaler Erregungskreise, wie sie im vegetativen und animalischen Nervensystem verbreitet sind.
Eigenreflex
Ein Eigenreflex ist ein monosynaptischer Reflex, bei dem Sensor und Effektor im gleichen Organ liegen und damit das Gegenteil eines Fremdreflexes. Meist ist beim Eigenreflex der Sensor die Muskelspindel und der Effektor der Muskel selbst. Der Eigenreflex passt die Muskelspannung an, indem er starken Dehnungsreizen einen Kontraktionsimpuls entgegenstellt. Dazu geht der sensorische Reiz vom Hinterhorn des Rückenmarks direkt monosynaptisch zum Motoneuron, das über die Vorderwurzel das Rückenmark verläßt und am Muskel ein Aktionspotential auslöst. Eigenreflex sind nicht veränderbar, also etwa durch Training verminderbar. Bekannte Eigenreflexe sind:
- Achillessehnenreflex
- Adduktorenreflex
- Bauchdeckenreflex (Rectus abdominis)
- Bizepssehnenreflex
- Bizeps-femoris-Reflex
- Extensor-digitorum-Reflex
- Fingerbeugerreflex
- Masseterreflex
- Patellarsehnenreflex (PSR)
- Pektoralisreflex
- Pronatorenreflex
- Radiusperiostreflex
- Skapulohumeralreflex
- Tibialis-posterior-Reflex
- Trizepssehnenreflex
- Zehenbeugereflex
Fremdreflex
Ein Fremdreflex ist einer, bei dem Sensor und Effektor verschieden sind. Damit können Fremdreflexe nicht monosynaptisch sein.
monosynaptischer Reflex
Ein monosynaptischer ist einer, bei dem Sensor und Effektor derselbst Muskel sind, sie sind also Eigenreflexe.
Nervengeflechte (Plexus)
Somatische Nervenplexus
– Plexus cervicobrachialis, den man unterteilen kann in
– – Plexus cervicalis für die Muskulatur und Sensibilität von Hinterkopf und Hals, gebildet aus den Nervenwurzeln C1 bis C4
– – Plexus brachialis für die Muskulatur und Sensibilität von Schulter und Arm, gebildet aus den Nervenwurzeln C5 bis Th1
– Plexus lumbosacralis, den man unterteilen kann in
– – Plexus lumbalis für Hüfte und Bein, gebildet aus den Nervenwurzeln Th12 bis L4
– – Plexus sacralis gebildet vor allem aus den Nervenwurzeln L5 und S1, mit motorischen und sensiblen Fasern für das Bein; die meisten Fasern des Plexus sacralis vereinigen sich zum Nervus ischiadicus
– – Plexus pudendus mit vegetativen Nervenfasern für Blase, Geschlechtsorgane und Enddarm, gebildet aus den Nervenwurzeln S2 bis S4
– Plexus coccygeus steuert bis auf den inneren Afterschließmuskel und dem inneren Schließmuskel der Harnblase (diese werden vegetativ gesteuert) die Harn- und Stuhlentleerung. Nervenwurzeln S5, Co1, Co2
Wichtige Vegetative Nervenplexus
Im menschlichen Körper gibt es einige Nervengeflechte, die regional für die Koordination von Organtätigkeiten und Informationsweiterleitung zuständig sind. Teilweise wird die Bezeichnung Plexus verwendet, teilweise die Bezeichnung Ganglion.
– Plexus coeliacus im Oberbauch, das größte paravertebrale Ganglion, links und rechts der Aorta auf Höhe des Truncus aorticus (Durchgang durch das Zwerchfell) des Abgangs des Truncus coeliacus
– Plexus mesentericus superior im Mittelbauch
– Plexus mesentericus inferior/caudalis im Unterbauch
In der Nähe von Organen und mit starkem Bezug zu diesen finden sich noch weitere vegetative Plexus:
– Plexus caroticus externus für die Schweißdrüsen, die glatten Muskeln der Haarfollikel und Blutgefäße im Bereich von Kopf und Gesicht
– Plexus caroticus internus für die Augen (Musculus dilatator pupillae, Musculus orbitalis, Musculus tarsalis) und die Tränen- und Speicheldrüsen
– Plexus cardiacus am Herzen aus den Endästen des parasympathischen Nervus vagus
– Plexus pulmonalis in der Wand der Bronchien für Bronchien und Lunge
– Plexus gastricus mit parasympathischen Fasern für die Versorgung des Magens
– Plexus vesicalis mit parasympathischen Fasern für die Versorgung der Harnblase und der Geschlechtsorgane
– Plexus pelvinus für die parasympathische Versorgung des Enddarms (Peristaltik) und die parasympathische Versorgung des nicht der Willkürkontrolle unterworfenen inneren Darmschließmuskels (Erschlaffung)
– Plexus hypogastricus superior und Plexus hypogastricus inferior für die Innervation der Geschlechtsorgane (Samenblasen, Prostata, Samenleiter)
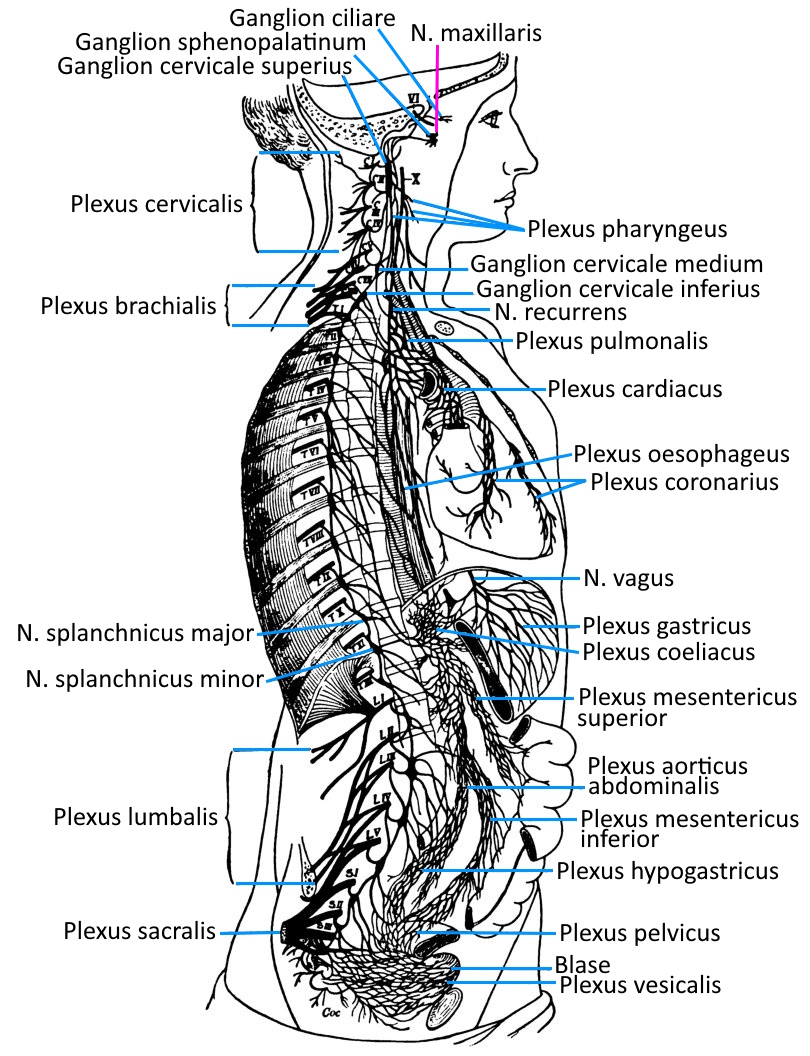
Der morphologischen Definition eines Nervenplexus nicht entsprechend, dennoch als vegetativer Nervenplexus zu betrachten ist das Darmnervensystem, eine über den gesamten Rumpfdarm verteilte Ansammlung von Neuronen; dies sind vor allem der Plexus submucosus (Meissner-Plexus) in der Tela submucosa des Rumpfdarmes und einen Plexus myentericus (Auerbach-Plexus) in der Tunica muscularis, zwischen Stratum circulare und Stratum longitudinale der glatten Darmmuskulatur.
Neuron
Eine Nervenzelle (Neuron) ist eine Zelle, die nebem dem Zellkörper (Soma, Perikaryon) meist auch (ggf. myelinisierte) efferente (zellulifugale) Fortsätze (Axon) und unmyelinisierte afferente (zellulipetale) Fortsätze (Dendrit).
Axon
Das Axon (Neurit) ist der Fortsatz einer Nervenzelle (Neuron), der Signale vom Zellkörper des Neurons weg leitet. Eine Nervenfaser ist ist die Gesamtheit aus dem Axon und seiner Umhüllung (Axolemm)
Dendrit
Ein Dendrit ist ein aus dem Zellkörper eines Neurons hervorgehender bis zu 100 µm langer Fortsatz, der der (überwiegend) Reizaufnahme dient. Er kann sich baumartig auffasern. Einige Dendriten weisen präsynaptische Spezialisierungen auf, die dendro-dendritische Synapsen ausprägen können. Auch elektrische Synapsen (Gap junctions) kommen zwischen Dendriten vor, genauso wie bidirektionale Synapsen (reziproke Synapsen).
Synapse
Eine Synapse ist eine anatomische Struktur, die die Übertragung eines Reizes von einem
Neuron auf ein anderes oder auf einen Effektor (z.B. Muskel, Drüse, Sinneszelle) erlaubt. Die Übertragung kann chemisch oder elektrisch (
Gap junction) geschehen. In beiden Fällen besteht die Synapse aus:
- Präsynapse (Sender)
- synaptischer Spalt
- Postsynapse (Empfänger)
Im Fall der chemischen Synapse setzt die Präsynapse
Neurotransmitter in den ca. 20-30 nm breiten synaptischen Spalt frei (Exozytose), die an Rezeptoren der Postsynapse andockenn. Bei der
Gap junction (elektrische Synapse) ist der Spalt nur 3,5 nm breit so daß Ionenkanäle (Connexone) den Reiz verzögerungsfrei (grundsätzlich bidirektional) leiten können. Vor allem bei der sehr schnellen Reizübertragung finden sich
Gap junctions. Synapsen unterteilen sich in erregende und hemmende Synapsen, weiter nach Effektor
- neuromuskuläre Synapse ( motorische Endplatte): mit einer Muskelzelle
- neuroglanduläre Synapse: mit einer Drüsenzelle
- interneurale Synapse: zwischen zwei Nervenzellen
- neurosensorische Synapse: mit einer sekundären Sinneszelle
und Kontakten
- axo-somatische Synapse: zwischen Axon und Zellkörper
- axo-axonische (axo-axonale) Synapse: zwischen zwei Axonen
- axo-dendritische Synapse: zwischen Axon und Dendritenbaum
- dendro-somatische Synapse: zwischen Dendriten eines Neurons und dem Körper eines anderen
- dendro-dendritische Synapse: zwischen Dendriten verschiedener Neurone
- somato-somatische Synapse: zwischen Zellkörpern eines Neurons und eines seiner unmittelbaren Nachbarn
- somato-axonale Synapse: zwischen Nervenzellkörper und dem Axon eines anderen Neurons
- somato-dendritische Synapse: zwischen Nervenzellkörper und Dendrit eines anderen Neurons
Die Austattung des Menschen mit Synapsen ist nicht fest und unveränderlich, sondern ändert sich im Sinne fortwährender Bildung neuer Synapsen (Synaptogenese), was als Neuroplastizität bezeichnet wird, und fortwährender Synapseneliminierung (Beseitigen nicht benutzter Synapsen).
Gap junction
Die Gap junction ist die elektrische Form einer Synapse. Ihr Spalt ist nur 3,5 nm breit, so daß Ionenkanäle (Connexone) den Reiz verzögerungsfrei (grundsätzlich bidirektional) leiten können. Vor allem bei der sehr schnellen Reizübertragung finden sich Gap junctions.
Neurotransmitter
Neurotransmitter sind die bei chemischen Synapsen von der Präsynapse in den synaptischen Spalt freigesetzten Stoffe. Je nach Kontext sind das:
- Adrenalin: an Adrenorezeptoren aufgenommen erhöht es Blutdruck, Herzfrequenz und arteriellen Gefäßtonus. Es wirkt im Glykogen- und Glucosestoffwechsel katabol und bewirkt den Abbau von von Triglyceriden im Fettgewebe.
- Acetylcholin: an nikotinische und muskarinische Rezeptoren bindender Neurotransmitter des ZNS und PNS, der in der motorische Endplatte Verwendung findet. Er bewirkt u.a. die Muskelkontraktion, hat steuernde Wirkung im VNS und ist an Gedächtnis- und Belohungsfunktionen beteiligt.
- Dopamin (Prolactin-Inhibiting-Hormon, PIH): wirkt an Adrenorezeptoren oder Dopaminrezeptoren (derzeit: D1 bis D5), steigert die Wirkung des Sympathikus, steigert die Durchblutung von Bauch- und Nierengefäßen zur Verbesserung der Nierenleistung, hemmt aber auch als Neurohormon des Hypothalamus die Freisetzung von Prolactin. Weiter wirkt Dopamin disinhibierend (die Hemmung hemmend)
- im Großhirn.
- Glutamin: ist eine nicht essentielle Aminosäure und mit 20% der freien Aminosäuren im Plasma weit verbreitetes Protein im Serum. Glutamin ist Blut-Hirn-Schranken-gängig und wirkt, zu Glutamat umgewandelt, als exzitatorischen (stimulierender) Neurotransmitter.
- Glycin: als Neurotransmitter des Hirnstamms und Rückenmarks am Glycinrezeptor inhibitorisch, am NMDA-Rezeptor hingegen neben dem hauptsächlichen Glutamat stimulierend
- GABA (?-Aminobuttersäure): Neurotransmitter des ZNS mit hauptsächlich inhibitorischer Wirkung an 3 verschiedenen GABA-Rezeptoren
- Serotonin: Neurotransmitter des PNS und ZNS, an 5-HT-Rezeptoren beteiligt an Thermoregulation, Schmerzempfindung, Schlafsteuerung, Ess- und Sexualverhalten, Gedächtnisleistung
- verschiedenene Peptide
Graue Substanz (Rückenmark) / spinale graue Substanz
Die graue Substanz des Rückenmarks besteht aus einem breiteren Vorderhorn und einem schmaleren Hinterhorn. Das Vorderhorn enthält die Enden der Pyramidenbahn, die Motoneurone und die Renshaw-Zellen, während das Hinterhorn den sensiblen Teil des Spinalnerven aufnimmt und die Informationen an das Vorderhorn, aber auch an das Gehirn weiterleitet.
- Wurzelzellen, darunter Motoneuronen der Skelettmuskulatur
- Binnenzellen (Eigenapparat, propriospinales System), die die graue Substanz nicht verlassen und aus verschiedenen Funktionsgruppen bestehen. So definieren sie etwa monosynaptische Reflexbögen oder verknüfpen Motoneuronen miteinander, womit sie neurologisch die Funktion der Antagonisten und Synergisten abbilden. Die Binnenzellen untergliedern sich in:
- Schaltzellen: Interneuronen desselben Segments
- propriospinale Neuronen, die ipsilateral in andere Segmente ziehen
- Neurone, die nach kontralateral ziehen. Sie definieren auch gekreuzte Reflexe.
- Strangzellen (Projektionsneuronen), die die graue Substanz verlassen und in die weiße Substanz ziehen.
Fremdreflexe basieren oft auf Assoziations-, Kommissuren- und Strangzellen.
Einige Begriffe
Allodynie
Allodynie ist ein durch einen inadäquaten Auslöser hervorgerufener Schmerz, meist Berührungsschmerz. Speziell erhöhte Sensitävitäten, etwa bei diabetischer Polyneuropathie oder Nervenschäden aus anderen Ursachen können zu diesem Symptom führen. So kann etwa bei Diabetes mellitus bereits die Berührung einer Bettdecke zu allopathischem Schmerz führen, nicht unähnlich der gesteigerten Empfindlichkeit bei Gicht.
Im Rahmen der Migräne ist die Allodynie ein Anzeichen einer Sensibilisierung des trigeminalen Nervennetzes. Beim Burning-Mouth-Syndrom treten Hyperalgesie und Allodynie an Zunge und im Mund auf. Die nach einer Gürtelrose auftretende Überempfindlichkeit ist ebenfalls eine Allodynie. Auch die Empfindlichkeit der Haut gegen Berührung bei einem Sonnenbrand (Insolination) ist eine Allodynie. Aber auch wiederholte Schädigungen wie Traumen können zu allodyn veränderter Schmerzempfindung führen.
exzitatorisch
Begriff aus der Neurophysiologie: erregend, stimulierend. Das Gegenteil ist inhibitorisch.
Hyperalgesie
Hyperalgesie ist ein gesteigertes Schmerzempfinden. Eine Hyperalgesie kann primär sein, sie ist dann peripher vermittelt und auf den Ort der Schädigung begrenzt, oder sekundär, dann ist sie vom ZNS vermittelt und die Schmerzempfindung kann über den Ort der Schädigung hinausreichen. Charakteristisch ist bei der primären Form die Überempfindlichkeit für Hitze durch eine verminderte Reizschwelle für die Nozizeption. Bei der sekundären Form liegt vor allem eine Überempfindlichkeit für mechanische Reize vor.
Hyperpathie
Die Hyperpathie ist eine zentrales (Thalamus) Schmerzsyndrom mit Sensibilitätsstörung in Form einer örtlich gesteigerten Schmerzreizschwelle. Die Schmerzen strahlen aus und halten lange an.
Die synaptische Übertragung ist plastisch verändert, repetitive Reize bewirken eine Langzeitpotenzierung, also eine Sensibilisierung der Schmerzbahnen, was auch den langen Nachhall des Schmerzes erklärt.
inhibitorisch
Begriff aus der Neurophysiologie: hemmend. Das Gegenteil ist exzitatorisch.
Kausalgie
Die Kausalgie (CRPS II, nicht zu verwechseln mit CRPS I, auch als Morbus Sudeck bezeichnet) ist eine Schmerzsyndrom, das infolge einer Läsion eines peripheren Nerven mit sympathischer Dysregulation auftritt. Die Schmerzempfindung ist nicht notwendigerweise auf den Ort der Verletzung begrenzt.
Die Klassifikation der International Association for the Study of Pain (IASP) beschreibt die Kausalgie als Ausschlußdiagnose bei gleichzeitigem Vorliegen der beiden Kriterien:
- kontinuierlicher Schmerz, Allodynie und Hyperpathie infolge Nervenschädigung, wobei der Schmerz das Versorgungsgebiet überschreiten kann
- Auftreten von Ödemen, veränderter Hautdurchblutung oder abnormaler Schweißsekretion im Schmerzgebiet
Die Kausalgie kann sich sensorisch, motorisch und autonom äußern und zeigt meist einen stechenden, brennenden Schmerz, der nicht unbedingt auf das Versorgungsgebiet des Nerven begrenzt ist. Allodynie oder Hyperpathie können begleitend auftreten, weiter Atrophie, Ödeme, Störungen der Schweißsekretion oder der Thermoregulation als Zeichen autonomer Schädigung. Dazu können auch Wachstumsstörungen der Haare oder Nägel gehören. Motorische Störungen können sich als Spasmen, Muskelschwäche, Dystonie oder Tremor äußern.
Kausalgien betreffen häufig N. medianus und N. tibialis.
Im Unterschied zur Kausalgie liegt bei CRPS I (Morbus Sudeck) ursächlich keine direkte Nervenschädigung vor, aber eine vorausgegangene Immobilisation oder ein Trauma.
Parästhesie
unangenheme, irritierende, aber nicht schmerzhafte Fehlempfindung oder Mißempfindung ohne adäquaten Auslöser, die häufig subjektiv als Brennen, Kribbeln, Ameisenlaufen, Nadelstichgefühl, pelziges Gefühl, Prickeln, Jucken, Schwellungsgefühl oder Kälte- oder Wärmeempfindung beschrieben wird. Hände und Finger sowie Füße sind am häufigsten davon betroffen. Die Parästhesien können unterteilt werden in
- transient: vorübergehend, bedingt durch Nervenkompression, vermimderte Blutzufuhr, Hyperventilation (durch Alkalose), Migräne
- chronisch persistierend: irreversible Nervenschäden, Polyneuropathie, z.B. im Rahmen von Diabetes mellitus (dort in 50% der Fälle) ; Hypothyreose (Schilddrüsenunterfunktion), Nervenengpasssyndrome, weiter medikamenteninduzierte Parästhesien
Trotz Parästhesie kann die Berührungsempfindlichkeit der Haut unverändert sein. Ursächlich sind Übererregbarkeiten peripherer sensibler Rezeptoren, Nervenfasern oder Bahnen des ZNS.
Hypästhesie
Eine Hypästhesie ist eine Sensibilitätsstörungen mit verminderter Druck- und Berührungsempfindung. Sie kann generalisiert oder lokalisiert auftreten. Nicht selten tritt die Hypästhesie zusammen mit einer Parästhesie auf. Im Falle einer Diskushernie (Bandscheibengeschehen) ist das bezügliche Dermatom betroffen, bei peripheren Nervenschädigungen das Versorgungsgebiet des Nerven. Die Ursachen können neben spinalen Geschehen, Radikulopathien, Durchblutungsstörungen auch Vergiftungen, Hirninfarkte oder Traumata mit Betreff von Nervenplexus sein.
Blut-Hirn-Schranke
Die Blut-Hirn-Schranke reguliert den Stoffaustausch zwischen Blut und Hirn, indem sie Stoffe am Durchtritt durch die Gefäßmembran hindert, die nicht ins Gehirngewebe gelangen sollen. Die involvierten Strukturen sind: Kapillarendothel, Basalmembran, Astrozytenfortsätze, Mikroglia, Perizyten. Dabei ist das Kapillarendothel mit den Tight Junctions, die die Diffusion auf ein Minimum beschränken und auch einen geringeren Vesikeltransport ausführen, besoners wichtig. Transponder und Rezeptoren sorgen hingegen dafür, daß wichtige Stoffe wie Glukose, Aminosäuren, Nukleoside und einige Neurotransmitter passieren können. Fettlösliche Substanzen können nur passieren, wenn ihr Molekulargewicht unter unter 500 Dalton liegt, das sind u.a. Nikotin, Alkohol, Blutgase, aber auch Narkotika wie Halothan. Ionen und polare Stoffe wie etwa Glukose brauchen spezielle Transportersysteme um die Blut-Hirn-Schranke zu passieren. Damit wird sichergestellt, daß die Zusammensetzung der interstitiellen Flüssigkeite des Gehirns weitgehend konstant und passend bleibt. Auf der anderen Seite wird auch ein unkontrolierter Austritt von Neurotransmittern aus dem Gehirn ins Blut verhindert. Die Blut-Hirn-Schranke ist in gewissem Umfang beeinflußbar und für pathogene Prozesse anfällig. Bei Erkrankungen wie Parkinson, Alzheimer, Chorea-Huntington, Epilepsie, Kopfschmerz, MS finden sich Veränderungen der Blut-Hirn-Schranke. Eine Analogie findet sich in Form der Blut-Rückenmark-Schranke beim Rückenmark.
Cauda equina
von lat.: Pferdeschwanz bezeichnet die nach Ende (Conus medullaris, etwa Höhe L1) des Rückenmarks pferdeschwanzartig nach kaudal in Richtung Kreuzbein weiter verlaufenden Nervenwurzeln der Spinalnerven, die durch ihre entsprechenden Zwischenwirbellöcher die Wirbelsäule verlassen.
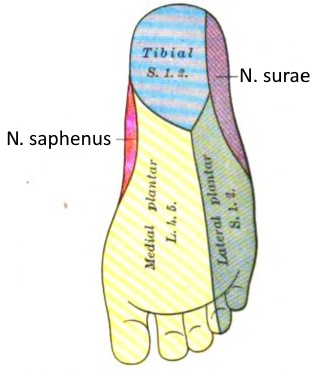
Dermatom
Ein Dermatom ist das von einem Spinalnerven versorgte Hautgebiet.
Siehe diese Abbildung. Die scheinbar willkürlich den Spinalnerven zugeordneten Dermatome erschließen sich sofort, wenn der Mensch in den Vierfüßlerstand geht: sie haben sich seit den Zeiten der tetrapoden Vorgänger nicht verändert.
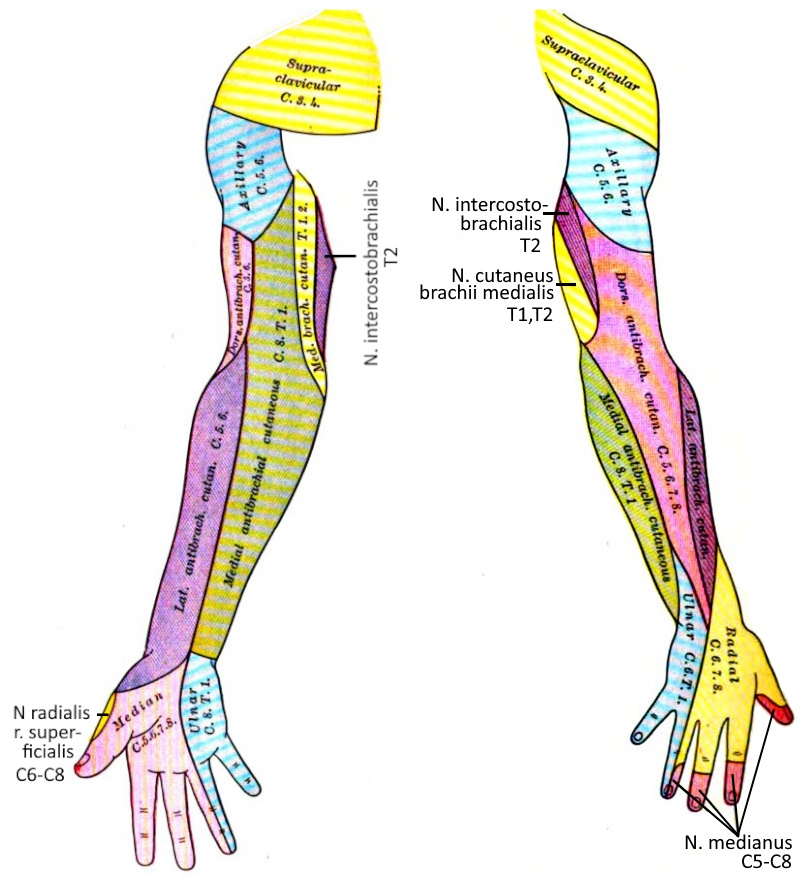
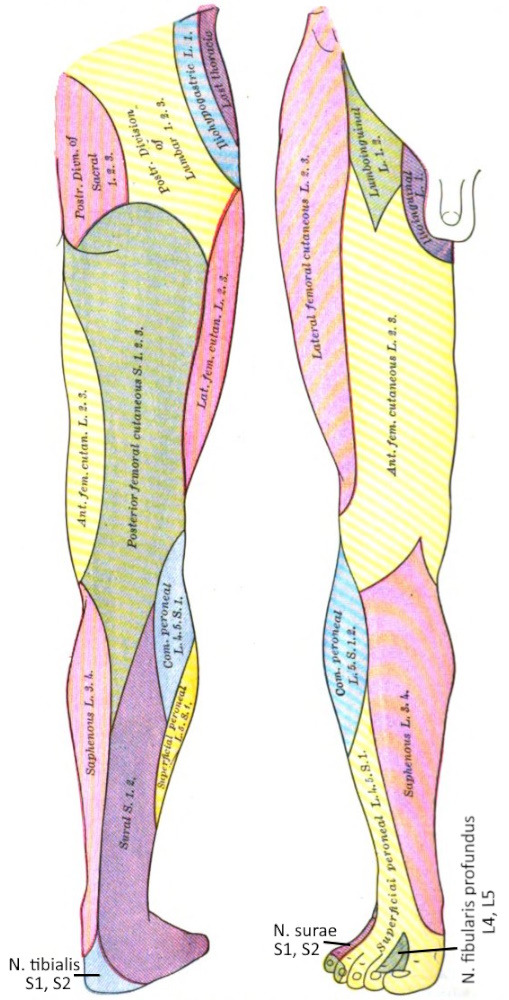
Golgi-Sehnenorgan
Nervengeflecht am Übergang des kontraktilen Muskelbauches zur Sehne, das den Spannungszustand (entspricht i.w. der
Sehnenkraft des Muskels) an das ZNS meldet. Im Sinne einer autogenen Hemmung wird das Motoneuron dieses Muskels gehemmt, also der Reiz zu weiterer Kontraktion gedämpft, gleichzeitig aber auch über erregende Schaltneurone (Interneurone) der Antagonist angeregt. Die autogene Hemmung dient der Regulation der Muskelspannung und dem Schutz vor Überlastung. Das Golgi-Sehnenorgan zählt zu den Propriozeptoren.
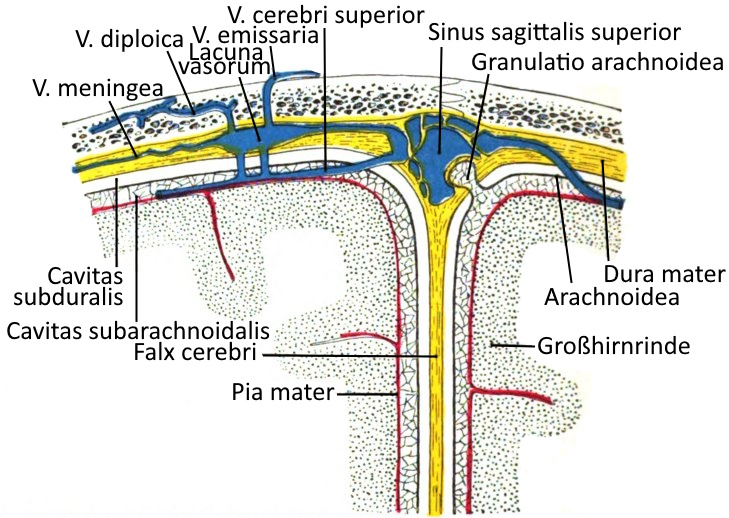
Hirnhäute
Die Hirnhäute sind Bindegewebsschichten, die das gesamte Gehirn umhüllen und sich kaudal des Foramen Magnum als Rückenmarkshäute fortsetzen als Dura mater spinalis, Arachnoidea spinalis und Pia mater spinalis.
Die Hirnhäute von außen (superfiziell) nach innen (profund):
Dura mater
Die direkt unter dem Schädelknochen liegende Dura mater besteht aus einem äußeren Blatt (Stratum periostale) und einem inneren Blatt (Stratum meningeale). In ihr liegen die Vv. meningeae, die Lacunae varosum und der Sinus sagittalis superior. Die Granulationes arachnoideae, nach superfiziell ausgerichtete Ausstülpungen der Arachnoidea, ragen in die Dura mater hinein. Im Bereich des Gehirns ist das Periost der Schädelknochen mit der Dura mater verwachsen, im Rückenmark liegt dazwischen der Epiduralraum. Ein Subduralraum zwischen der Dura mater und der nächst-profunderen Hirnhaut, der Arachnoidea tritt physiologisch nicht auf, nur postmortem und unter gewissen pathologischen Bedingungen. Die Dura mater bildet median eine ins Gehirn gerichtete Doppelung aus, den Falx cerebri, der das Gehirn in seine beiden Hemisphären teilt sowie den Falx cerebrelli, der die Kleinhirnhälften unterteilt, und das Tentorium cerebelli.
Arachnoidea
Zwischen der mittleren der klassischen drei Hirnhäute, der Arachnoidea, und der direkt dem Cortex aufliegenden profundesten Hirnhaut, der Pia mater, liegt der mit Liquor gefüllte Subarachnoidalraum, die Cavitas subarachnoidalis.
Nach Untersuchungen aus 2023 von Møllgård et al. ist der Subarachnoidalraum durch eine dünne Membran, die als Subarachnoidal Lymphatic-like Membrane bezeichnet wird, in zwei Domänen geteilt. Diese Membran soll den Liquor filtern und eine Rolle bei Entzündungsreaktionen und der Abwehr von Erregern spielen.
Pia mater
Die Pia mater ist die profundeste der Hirnhäute und liegt direkt auf dem Cortex. Zwischen ihr und der superfizielleren Hirnhaut, der Arachnoidea, liegt der mit Liquor gefüllte Subarachnoidalraum. Die Arachnoidea stülpt sich in den Granulationes arachnoideae in die Dura mater hinein.
Hirnnerven
Die Hirnnerven treten paarig aus dem Schädel aus und leiten Signale von oder zum Gehirn.
- I N. olfactorius leitet Signale von der Nase zum Gehirn und ermöglicht das Riechen
- II N. opticus leitet Signale vom Auge zum Gehirn und ermöglicht das Sehen
- III N. oculomotorius steuert Augenbewegungen, den Lidheber und die Iris (Regenbogenhaut)
- IV N. trochlearis steuert den schrägen oberen Augenmuskel
- V N. trigeminus unterteilt sich in ophtalmicus, maxillaris und mandibularis, leitet Signale aus dem Gesicht ans Hirn und steuert die Kaumuskulatur
- VI N. abducens steuert den lateralen Augenmuskel
- VII N. fascialis steuert die mimische Muskulatur und den M. stapedius (Mittelohr), leitet geschmackssensorische Reize der vorderen zwei Drittel der Zunge zum Gehirn, innerviert alls Kopfdrüsen mit Ausnahme der Parotis
- VIII N. vestibulococclearis leitet Signale der Hörschnecken und des Gleichgewichtsorgans ans Gehirn
- IX N. glossopharyngeus innerviert die Rachenmuskeln und steuert das Schlucken, leitet sensorische Reize des hinteren Drittelns der Zunge zum Hirn
- X N. vagus wichtigster Nerv des Parasympathikus, steuert viele innere Organe mit, auch das Herz
- XI N. accessorius steuert den Trapezius und den Sternocleidomastoideus
- XII N. hypoglossus steuert die Bewegungen der Zunge
Zuweilen wird der N. terminalis als Nullter Nirnnerv (vermutlich Wahrnehmung von Pheromonen) bezeichnet und der zum N. fascialis gehörige N. intermedius als 13. Hirnnerv.
Medulla oblongata
Die Medulla oblongata (verlängertes Mark: intrakranielle Verlängerung des Rückenmarks) ist der am weitesten kaudal gelegene dreiteilige Teil des Hirn, der kranial an die Pons grenzt und kaudal an das Rückenmark, wobei meist der Abgang des 1. Spinalnerven als die Grenze angenommen wird. Die Medulla oblongata ist die wichtigste Steuerzentrale für viele Vitalfunktionen, darunter Parameter des Blutkreislaufs, der Atmung, Nies-, Schluck, Sauck- und Hustenreflex, das Erbrechen (Retroperistaltik). Weiter liegen hier einige Rezeptoren für die Regulierung des Säure-Base-Haushalts. Ein Teil der Pyramidenbahn, insbesondere die Decussatio pyramidum leigt in der Medulla oblongata.
Intramuskuläre Koordination
Die Intramuskuläre Koordination ist das Zusammenspiel der Innervierung mit der Muskulatur und neben der Hypertrophie die wichtigste Größe, die die Maximalkraft eines bestimmten Muskels bestimmt. Dieser Faktor ist besonders für Sportler wichtig, die einen Kraftzuwachs ohne Massezunahme wünschen, wie etwa Ausdauersportler (Triathlon, Running) oder Krampfsportler. Auch für andere Maximalkraft-Sportarten wie Gewichtheben oder Schnellkraft-Sportarten wie Sprungdisziplinen ist dies bedeutsam. Im spezifischen Training wird dabei im Lastbereich von 85-100% des 1-RM mit Wiederholungszahlen zwischen 1 und 3 gearbeitet (3-6 Sätze).
Ischiasnerv
Als „Ischiasnerv“ werden der gemeinsam bindegewebig verpackten Nervus fibularis communis und Nervus tibialis bezeichnet. Beide treten unabhängig voneinander aus dem Plexus lumbosacralis aus, gehen aber durch das in einer gemeinsamen Hülle. Der Ischiasnerv versorgt die untere Extremität, dabei werden sämtliche Beuger (Ausnahme: M. biceps femoris caput breve) des Kniegelenks und OSG vom Nervus tibialis versorgt und die Strecker und Pronatoren der Sprunggelenke vom Nervus fibularis communis. Wird der Nerv in seinem Verlauf gereizt oder komprimiert, seien es die zugrundeliegenden Spinalnerven oder der Ischiasnerv in seinem Verlauf im dorsalen Hüftbereich, kommt es zu Störungsbildern wie der Ischialgie oder Lumbalgie bzw. ischialgiformen oder lumbalgiformen Schmerzen. Diese können allerdings auch schlicht durch Kompression durch einen Muskel hervorgerufen werden wie beim Piriformis-Syndrom/Deep Gluteal Syndrom DGS. Ähnliche Störungsbilder entstehen auch, wenn die bezüglichen Nerven noch im Rückenmarkskanal komprimiert werden wie etwa bei einer Spondylolisthesis (Wirbelgleiten) oder einer Spinalkanalstenose, so dass diese Bilder differentialdiagnostisch unterschieden werden müssen. Teilweise gelingt dies schon mit Hilfe von Anamnese und Provokationstests, sonst muss Bildgebung wie MRT bemüht werden. Reizungen des Ischiasnervs können auch durch Kälteeinwirkung oder Druck (teils dem DGS zugehörig) ausgelöst werden. Bei einem Facettensyndrom treten ähnliche Schmerzen auf, die jedoch pseudoradikulär und nicht radikulär sind und keine muskulären oder sensitiven Ausfälle verursachen.
Kennmuskeln
Kennmuskeln sind Muskeln, die in der klinischen Testung stellvertretend für ein Myotom und einen Spinalnerven getestet werden, etwa wenn der Verdacht auf Schäden an einem WS-Segment besteht.
- C4: Diaphragma
- C5: Deltoideus, Infraspinatus, Supraspinatus, Rhomboiden
- C6: Bizeps, Brachioradialis
- C7: Trizeps, Pronator Teres, Extensor carpi radialis, Flexor carpi radialis, Pectoralis major
- C8: Interossei, Abduktor pollicis brevis, Abduktor digiti minimi, Flexor carpi ulnaris, Flexor pollicis brevis
- Th10-Th12: Bauchmuskeln
- L1: Cremaster
- L3: Quadrizeps, Iliopsoas, Adduktor longus, Adduktor brevis, Adduktor magnus
- L4: Quadrizeps femoris: Vastus lateralis
- L5: Fibularis longus, Extensor hallucis longus, Tibialis anterior, Tibialis posterior, Gluteus medius
- S1: Trizeps surae, Gluteus maximus
- S2: Flexor digitorum brevis
- S3/S4: Bulbospongiosus
- S4/S5: Sphinkter ani externus
Einige der Kennmuskeln sind mit sehr leichten Tests prüfbar:
- Quadrizeps: Kniebeuge
- Trizeps surae: Zehenstand
- Tibialis anterior: Fußballenstand
Motoneuronen
Ein Motoneuron ist eine efferente Nervenzelle (Neuron) im Vorderhorn des Rückenmarks, die mit ihrem Axon direkt oder indirekt einen Skelettmuskel oder eine Drüse innerviert. Die Motoneurone besitzen die längsten Nervenfasern im ganzen Körper und bilden die efferenten Nervenbahnen. Eine Einteilung der Motoneurone ist die in viszerale Motoneurone (steuern die glatte Muskulatur) und somatische Motoneurone (steuern die quergestreifte Muskulatur). Wie viele Neuronen besitzen die Motoneurone Soma (Zellkörper), Axone (sendend) und Dendriten (empfangend). Meist besitzen Motoneuron ein Axon und mehrere Dendriten . Zur schnellen Signalübertragung sind die Axone mit Myelinscheiden ummandelt. Das Axone verästelt sich in einen Baum, das Telodendron, das im Muskel verschiedene Fasern innerviert. Dazu setzen axonterminale Endknöpfchen den jeweiligen Neurotransmitter frei, der von den motorischen Endplatten der Muskeln aufgenommen wird. Das Motoneuron zusammen mit den zugehörigen Muskelfasern wird als motorische Einheit bezeichnet. Die Leitungsgeschwindigkeit von Motoneuronen beträgt zwischen 2-30 m/s (kleine gamma-Motoneuronen) bis 60-12 m/s (alpha-Motoneuronen).
Mit wenigen Ausnahmen werden die Muskeln des Bewegungsapparates nicht direkt vom Gehirn gesteuert sondern über zwei Motoneuronen, das UMN und das LMN, auch als 1. Motoneuron und 2. Motoneuron bezeichnet. Das obere Motoneuron (upper motoneuron, UMN oder 1. Motoneuron) und das untere Motoneuron (lower motoneuron, LMN oder 2. Motoneuron). Als Motoneuronen werden Nervenzellen bezeichnet, die eine direkte oder indirekte Kontrolle über einen Muskel ausübt. Hierbei unterscheidet man in somatische Motoneuronen (innervieren Skelettmuskeln) und viszerale Motoneuronen (innervieren glatte Muskulatur).
Störungen des 1. Motoneurons (UMN) führen zu in der Regel einer spastischen Lähmung, Störungen des 2. Motoneurons (LMN) zu einer schlaffen Lähmung
UMN
Neuronen der Hirnrinde und des Hirnstamms, die ihre Signale an Interneuronen und LMN weitergeben. Die Zellkerne dieser Nerven des UMN liegen überwiegend im motorischen Kortex des Gehirns, seine Axone als verschiedene Tracti in der Pyramidenbahn und der extrapyramidalmotorischen Bahn zu den LMN im Vorderhorn der grauen Substanz des Rückenmark.
LMN
In jedem WS-Segment verlassen Axone des LMN über den Spinalnerven das Rückenmark und damit die WS. Diese ziehen in mehreren Ästen in sein Versorgungsgebiet (Myotom: die Muskulatur, die von einem Spinalnerven versorgt wird und in Analogie Dermatom: das Hautareal, welches von einem Sinalnerven versorgt wird). Das LMN ist der efferente Schenkel aller Bewegungen und Reflexe (siehe unten) und innerviert direkt die Muskeln. Neurotransmitter zwischen UMN und LMN ist Glutamat.
Myotom
Ein Myotom ist die Menge aller von einem Spinalnerven versorgten Muskeln.
Nervenkompressions-Syndrom
Syndrom u.a. mit Schmerzen, Sensitivitätsstörungen wie Taubheit, Kribbeln, verminderter Empfindung sowie Innervationsstörungen, welches durch Druck auf einen Nerven entsteht. Dies kann ein gerade aus dem Rückenmark ausgetretener Spinalnerv sein wie beim Bandscheibengeschehen, dann spricht man von einem Nervenwurzelkompressionssyndrom bzw. einer Radikulopathie (lat „Radix“: Wurzel) oder ein weiter in der Peripherie liegender Nerv, etwa wenn Sehnen im Bereich einer physiologischen Engstelle zwischen Knochen anschwillen und auf einen Nerven drücken, wie dies beim Kubitaltunnelsyndrom (betroffen: N. ulnaris), Tarsaltunnelsyndrom (betroffen: N. tibialis) und beim Karpaltunnelsyndrom (betroffen: N. medianus) der Fall ist. Ein anderes verbreitetes Nervenkompressionssyndrom ist das Morton-Neurom, welches meist im Rahmen eines Spreizfußes auftritt und eine Metatarsalgie verursacht.
Nervenwurzel
Nervenwurzeln sind die segmentweise sich vereinigenden und aus dem Rückenmark austretenden Anteile der Spinalnerven. Druck auf diese kann zum Nervenwurzelkompressionssyndrom und im späteren Verlauf des Nerven zum Nerven(wurzel)kompressionssyndrom führen.
Nervenwurzelkompressions-Syndrom
Ein durch Druck auf einen aus der WS austretenden Spinalnerven verursachtes Nervenkompressionssyndrom. Beschreibung siehe dort.
neuroradikulär
Beschwerden, die durch ein Nervenwurzelkompressions-Syndrom einer oder mehrere aus der Wirbelsäule austretenden Nervenwurzeln ausgelöst werden, kurz wird dann auch von radikulär gesprochen, siehe auch die dortigen Erklärungen.
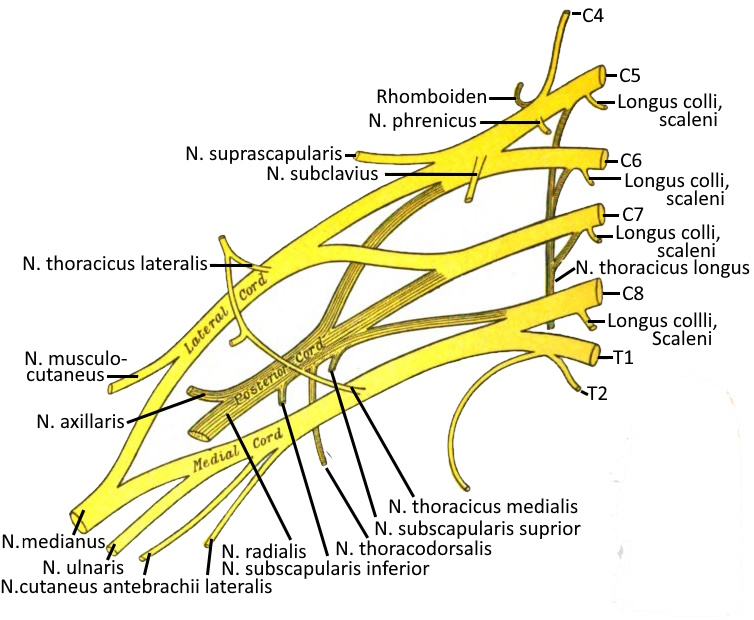
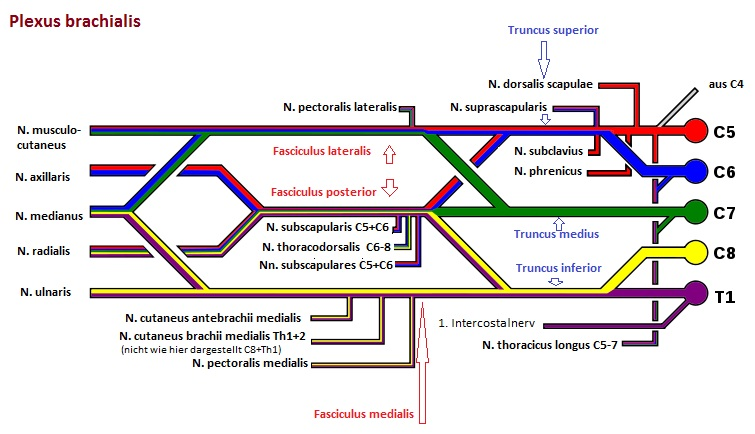
Plexus brachialis
Der Plexus brachialis (Armgeflecht) ist als Teil des PNS ein Nervenplexus aus den ventralen Ästen der Spinalnerven der letzten vier HWS-Segmente und des ersten BWS-Segments (C5-Th1) sowie kleinerer Bündel von C4 und Th2. Eine Kompression des Plexus brachialis kann zum Thoracic Outlet Syndrom führen.
Supraklavikulär gehen aus Truncus superior (C5, C6), Truncus medius (C7) und Truncus inferior (C8, Th1) hervor: Rami musculares, N. suprascapularis, N. dorsalis scapulae, N. thoracicus longus, N. subclavius.
Das größte Teil des Plexus brachialis liegt infraklavikular, dort gehen aus Fasciculus lateralis, Fasciculus medialis und Fasciculus posterior hervor:
N. pectoralis medialis und N. pectoralis lateralis (Fasciculus lateralis bzw. medialis), N. musculocutaneus (Fasciculus lateralis), N. medianus (Fasciculus lateralis und medialis), N. ulnaris (Fasciculus medialis), N. cutaneus brachii medialis (Fasciculus medialis), N. cutaneus antebrachii medialis (Fasciculus medialis), N. axillaris (Fasciculus posterior), N. radialis (Fasciculus posterior), N. subscapularis (Fasciculus posterior), N. thoracodorsalis (Fasciculus posterior)
Plexus lumbosacralis
Zusammenfassender Begriff für Plexus lumbalis und Plexus sacralis, die sich aus Anteilen der Spinalnerven der Segmente von T12, L1 bis L5 und S1 bis S4 zusammensetzen.
Plexus lumbalis
Der Plexus lumbalis ist als Teil des PNS ein Nervenplexus aus anterioren Ästen der Spinalnerven der Segmente L1 bis L3, zusätzlich aus Teilen von T12 und L4. Von Plexus lumbalis und Plexus sacralis gehen die Nerven des Beckens und der Beine aus.
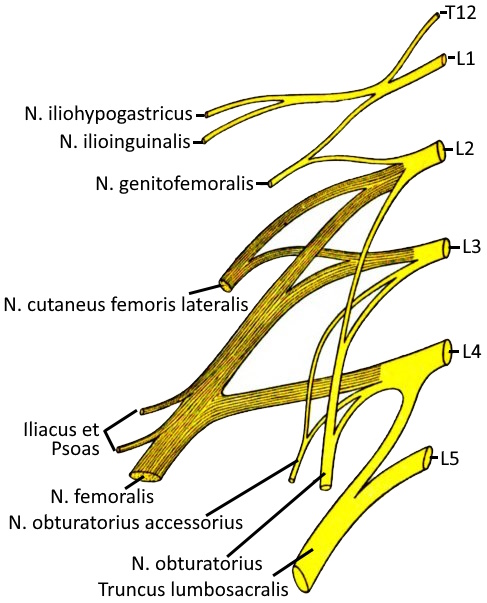
Plexus sacralis
Der Plexus lumbalis ist als Teil des PNS ein Nervenplexus aus anterioren Ästen der Spinalnerven der Segmente L5 bis S3, zusätzlich aus Teilen von L4 und S4. Von Plexus sacralis und Plexus lumbalis gehen die Nerven des Beckens und der Beine aus.
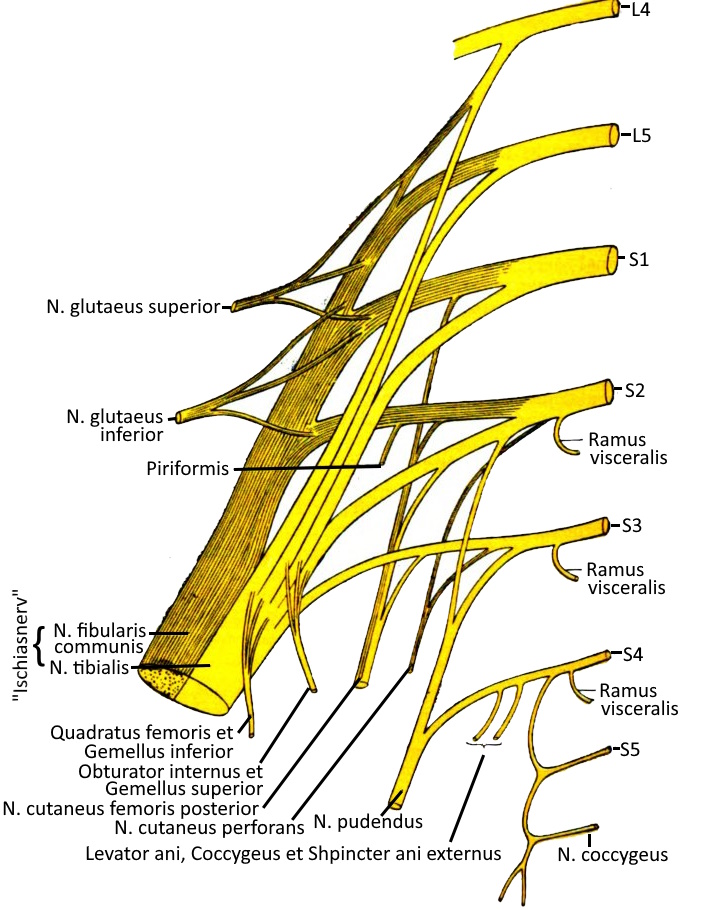
Propriozeption
Eigenwahrnehmung des Körpers unabhängig von äußeren Sensoren, also den 5 Sinnen. Propriozeption ermöglicht es, die Stellung des Körpers im Raum und die Stellung der einzelnen Körperteile zueinander wahrzunehmen, genauso die wie Spannung der Muskulatur und die ausgeübte Kraft. Dabei wird unterschieden zwischen
- Stellungsinn (Joint Position Sense): Empfinden für die geometrische Stellung des Körpers und der Gelenke
- Bewegungssinn (Kinethesia): kontinuierliche Empfindung für Veränderungen der Lage des Körpers oder von Körperteilen
- Kraft- und Widerstandssinn: Empfindung von Zug und Druck.
Die dafür verantwortlichen Sensoren werden Propriozeptoren genannt, dies sind:
- Muskelspindel: im Muskel parallel zu den Muskelfasern angeordnete Fasern, die mit statischen Kernsackfasern das Proportionalverhalten, also die absoluten Länge eines Muskels erfassen und mit den dynamischen Kernsackfasern das Differentialverhalten, also die Längenänderung.
- Sehnenspindel (auch: Golgi-Organ, Golgi-Sehnenrezeptor): im Übergangsbereich zwischen Muskel- und Sehnenfasern angesiedelte langsam-adaptierenden Spannungssensoren, Basis der Eigenreflexe
- sensible Rezeptoren in Gelenkkapsel, Bändern, Knochenhaut
Im Gegensatz zur Propriozeption ermöglicht die Viszerozeption die Wahrnehmung der inneren Organe. Beide zusammengenommen wird auch von Interozeption gesprochen. Dazu sind verschiedene Propriozeptoren vorhanden.
Man kann zwischen einer bewußten Propriozeption unterscheiden, die etwa bei bewußt und gezielt ausgeführten Bewegungen ausgewertet wird wie Balancieren oder Yogahaltungen und einer unbewußten, die in mechanischen Verrichtungen wie Gehen oder Treppesteigen ausreicht.
Propriozeptoren
Die Rezeptoren, die die Propriozeption ermöglichen, dies sind:
- Muskelspindel: im Muskel parallel zu den Muskelfasern angeordnete Fasern, die mit statischen Kernsackfasern das Proportionalverhalten, also die absoluten Länge eines Muskels erfassen und mit den dynamischen Kernsackfasern das Differentialverhalten, also die Längenänderung.
- Sehnenspindel (auch: Golgi-Organ, Golgi-Sehnenrezeptor): im Übergangsbereich zwischen Muskel- und Sehnenfasern angesiedelte langsam-adaptierenden Spannungssensoren, Basis der Eigenreflexe
- sensible Rezeptoren in Gelenkkapsel, Bändern, Knochenhaut
Pyramidenbahn (Tractus pyramidalis)
Die ist das pyramidalmotorische System der Willkürmotorik, das die Signale des motorischen Kortex zu den willkürlichen Muskeln dse Körpers leitet. Es unterteilt sich in
Tractus corticospinalis: zu den α-Motoneuronen der peripheren Muskulatur und
Tractus corticonuclearis: zu den motorischen Hirnnervenkernen
Im engeren Sinne wird unter Pyramidenbahn nur der Tractus corticospinalis verstanden. In der Pyramidenkreuzung keruzen 70-90% der Fasern als Tractus corticospinalis lateralis auf die kontralaterale Seite, der Rest verläuft als Tractus corticospinalis anterior weiter nach distal. Die Pyradimenbahn steuert vor allem die Feinmotorik, die gewohnheitsmäßig eingeschliffene Grobmotorik wird über das extrapyramidalmotorischen System geleitet. Beide gehören zum somatomotorischen System, sind also somatische und motorische Fasern.
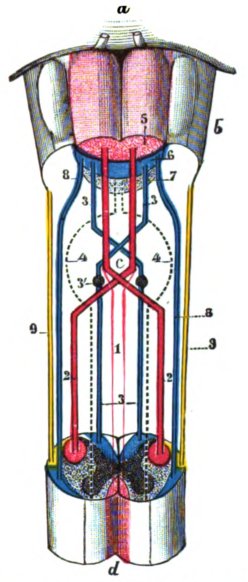
Pyramidenbahnzeichen
Neurologische Symptome, die auf eine Schädigung der Pyramidenbahn hinweisen. Es sind etliche für die untere Extremität bekannt: Babinski-Reflex, Bechterew-Reflex, Chaddock-Reflex, Gordon-Reflex*, Oppenheim-Reflex, Mendel-Bechterew-Reflex, Plantarmuskelreflex, Rossolimo-Reflex*, Piotrowski-Reflex, Fußrückenreflex*, Strümpell-Reflex, aber auch einige für die obere Extremität: Gordon-Fingerspreizzeichen*, Trömner-Reflex*, Wartenberg-Reflex, nichterschöpfbarer Handklonus, von denen die mit * gekennzeichneten als unsichere Zeichen gelten.
Störungen des 1. Motoneurons (UMN) führen zu in der Regel einer spastischen Lähmung, Störungen des 2. Motoneurons (LMN) zu einer schlaffen Lähmung
Rückenmark
(lat. medulla spinalis oder medulla dorsalis) im Spinalkanal verlaufender Teil des zentralen Nervensystems. Das Rückenmark endet kaudal als Conus medullaris (Markkegel) im Bereich L1 / L2, dort verlaufen die Nerven einzeln weiter als Cauda equina. Die Existenz eines Rückenmarks ist allen Wirbeltieren gemein. Es ist von Meningen (Hirnhaut, von außen nach innen: dura mater, arachnoidea, pia mater) umhüllt, die wiederum von Liquor (Gehirn-/Rückenmarksflüssigkeit) umspült werden. Kranial geht das Rückenmark aus der oberhalb des Foramen Magnum liegenden Medulla Oblongata hervor. Im Rückenmark befinden sich die grau und weiße Substanz, für eine eingehendere Beschreibung siehe z.B. Wikipedia.
Spinalkanal
Der Rückenmarkskanal, in dem das Rückenmark verläuft, und aus dem die Spinalnerven durch die Wirbellöcher austreten.
Spinalnerv
Die Spinalnerven sind die paarig (rechts/links) aus dem Rückenmark austretenden Nerven. Ab ihrem Austritt aus dem Rückenmark zählen sie zum PNS. Die Spinalnerven vereinen die vorderen und hinteren afferenten und efferenten Nervenwurzeln: Afferenzen mit sensiblen Informationen treten durch die hintere Nervenwurzel (Radix posterior) ein, Efferenzen mit motorischen Nervenfasern und teils auch Fasern des N. vagus treten durch die vordere Nervenwurzel aus. Druck auf eine Nervenwurzel bzw. den sie enthaltenden Spinalnerv kann zum Nervenkompressionssyndrom führen. Die Vereinigung der Nervenwurzeln erfolgt bereits im Rückenmarkskanal.
Liquor
Vom Plexus coroidei als Ultrafiltrat des Blutserums gebildete Körperflüssigkeit des ZNS, die in einem als Liquorraum bezeichneten System kommunizierender Hohlräume zirkuliert und dem Stoffwechsel (Ernährung und Entsorgung) des ZNS dadurch dient, daß sich die
interstitielle Flüssgkeit aus dem Liquor ableitet. In Analogie zur Blut-Hirn-Schranke gibt es hier eine Blut-Liquor-Schranke. Aufseiten der Entsorgung ist der Liquor die Entsprechung zum im Gehirn nicht vorhandenen Lymphesystem. Liquor ist zellarm, die größte Population stellen mit bis zu 3 / µl die Lymphozyten dar, selten sind auch Monozyten nachweisbar. Proteine sind gegenüber dem Blutserum ebenfalls massiv vermindert (etwa Faktor 200), lediglich Glukose liegt bei 50-70% de Serums. Die zirkulierende Gesamtmenge beträgt ca. 150 ml. Von der Tagesproduktion von 500-700 ml wird der Großteil an den Granulationes arachnoidales und den Nervenwurzeln resorbiert. Ein weiterer Teil fließt zusätzlich entlang der Hirnnerven und Spinalnerven in die Peripherie ab.
Eine weitere Funktion des Liquor ist es, eine Art Wasserkissen zum mechanischen Schutz des Hirns darzustellen. Außerdem erhält das Gehirn durch die Einbettung in Wasser hydrodynamisch einen Auftrieb, was den Druck der unteren Hirnpartien signifikant vermindert.
Diagnostisch wird der Liquor wichtig, wenn die Zahl der Leukozyten erhöht ist, was auf eine Entzündung hinweist, oder wenn Erythrozyten im Liquor auftreten, was auf eine Subarachnoidalblutung hinweist.
Parasympathikoton
Zustand erhöhter Erregung des Parasympathikus.
Sympathikoton
Zustand erhöhter Erregung des Sympathikus.
Vagusnerv (N. vagus)
Der N. vagus ist Gegenspieler des Sympathikus und wichtigster Teil des Parasympathikus. Er ist der 10. Hirnnerv und zieht als einziger aus dem Kopf in den Rumpf, daher auch sein Name „umherschweifender“. Er steuert u.a. die Verdaung und beruhigt das Herz, siehe dazu die Wirkungen des Parasympathikus und die Herzratenvariabilität (HRV).
vagoton
Zustand erhöhter Erregung des N. vagus.
Schmerz
Schmerz ist eine komplexe subjektive Sinneswahrnehmung, die als akutes Geschehen den Charakter eines Warn- und Leitsignals aufweist und in der Intensität von unangenehm bis unerträglich reichen kann. Als chronischer Schmerz hat es den Charakter des Warnsignales verloren und wird heute als eigenständiges Krankheitsbild (Chronisches Schmerzsyndrom) gesehen und behandelt. (Wikipedia)
IASP (International Association for the Study of Pain): Schmerz ist ein unangenehmes Sinnes- oder Gefühlserlebnis, das mit einer tatsächlichen oder potentiellen Gewebeschädigung einhergeht, bzw. mit Begriffen einer solchen beschrieben wird.
ICD (International Statistical Classification of Diseases and Related Health Problems; aktuell ICD-10, ab 2022: ICD-11, Klassifikationssystem für medizinische Diagnosen der WHO): Schmerz ist eine komplexe Sinnesempfindung, die durch die Erregung von Schmerzrezeptoren hervorgerufen wird. Häufig kommt Schmerz auch unter Beteiligung weiterer Sinne (Druck- und Temperatursinn) zustande, ebenso spielt die psychische Verfassung eine Rolle. Man unterscheidet verschiedene Schmerzqualitäten wie brennenden, bohrenden, klopfenden oder stechenden Schmerz.
Allgemein gilt Schmerz als ein biologisches Alarmsignal und stellt eine Schutzfunktion des Körpers dar. Schmerz ist in der Medizin ein wichtiges Symptom, kann aber speziell bei psychosomatischen Erkrankungen ein eigenständiges Krankheitsbild darstellen.
Nozizeptor
Freie Nervenendigungen in Geweben, die Schmerz aufnehmen heißen Nozizeptoren. Es gibt sie in der Haut aber auch fast jedem anderen Gewebe. Sie reagieren auf verschiedene Bedingungen, etwa mechanische (Druck), chemische und thermische. Signale der Nozizeptoren führen meist, aber nicht immer zu einer Schmerzempfindung. Hingegen beruhen organische Schmerzen immer auf den Signalen von Nozizeptoren. Siehe Nozizeptorenschmerz
Schmerzformen
Nozizeptorenschmerz
Nozizeptoren (freie Nervenendigungen) reagieren z.B. chemisch, mechanisch, thermisch und zeigen kaum Adaption im Gegensatz zu Rezeptoren
– Somatischer (den Körper betreffend) Nozizeptorenschmerz entsteht durch Reizung der Nozizeptoren der Haut, Schleimhaut, Knochen, Skelettmuskulatur, Bänder, Sehnen, Muskulatur, Bindegewebe, Hohlorgane u.a. und ist scharf begrenzt, gut lokalisierbar und stechend bis brennend, permanent oder an- und abschwellend, der Mensch reagiert meist mit Bewegungsvermeidung/Schonhaltung. Unterscheide sind wahrnehmbar zwischen Oberflächenschmerz (Haut) und Tiefenschmerz. Weiter: Erster Oberflächenschmerz (kurz, hell, scharf, gut lokalisierbar, markhaltige Fasern), zweiter Oberflächenschmerz (diffus, dumpf, brennend, langsam abklingend, marklose Fasern, entspricht neurophysiologisch dem Tiefenschmerz)
-Viszeraler (die Eingeweide betreffend) Nozizeptorenschmerz bei der Reizung von Nozizeptoren in den inneren Organen des Becken-, Bauch und Brustraums. Diese Schmerzen sind drückend, ziehend, dumpf, brennend, wellenartig, bohrend; dauernd oder kolikenartig, krampfartig, wellenförmig; diffus nicht gut lokalisierbar. Beispiele: Dehnungen von Hohlorganen, Spasmen glatter Muskulatur, Entzündungen, Durchblutungsstörungen
Neuropathischer/neurogener Schmerz (Reizung/Kompression/Schädigung peripherer Nerven oder Kompression von Nervenwurzeln im Bereich der WS)
a. kurz/akut: schneidend, stechend und attackenweise auftretend, blitzartig einschießend, nicht gut lokalisierbar, empfundene Lokalisation möglicherweise distal des eigentlichen Geschehens.
b. Dauerschmerz: brennend oder bohrend
Beispiele: Amputationens-Phantomschmerz, Herpes Zoster-Neuralgie, Polyneuropathie.
Schmerz durch funktionelle Störungen
z.B. durch vaskuläre Fehlregulation, Muskelverspannungen, Hartspann, auch psychosomatische Schmerzen. Dieser Schmerz wird auch als funktioneller Schmerz bezeichnet.
Chronische Schmerzsyndrome (>= 6 Monate)
1. Entzündungsschmerzen (häufig chemisch induziert)
2. spastische (übermäßige Kontraktion der Muskulatur)
3. Nervenschmerzen (Irritation von Nerven des ZNS/PNS)
4. Fehlregulationsschmerzen (Fehlfunktion der Motorik, z.B. Überspannung von Muskulatur, oder des sympathischen NS, z.B. Ischämie durch Vasospasmus, Fehlregulationen von Neurotransmittern, z.B. Migräne)
5. psychomotorische Schmerzen (Ausdruck psychomentaler Zustände)
Das NS besteht aus einem der Willkür unterworfenen Teil („animales“ NS) und einem ihr nicht primär unterworfenen „autonomen“ oder „vegetativen“ NS mit den drei Bereichen
– sympathisches NS (Energieentladung, Handlung, „ergotrop“)
– parasympathisches NS (Energiespeicherung, Erholung, Aufbau, „trophotrop“)
– intramurales (Wände der Hohlorgarne)
Muskelspindel, Muskelrezeptoren (Dehnungsrezeptoren, Mechanorezeptoren)
Die Muskelspindel ist ein intramuskuläres Sinnesorgan (Propriozeptor), das die relative Muskellänge erfasst, was einer Messung der Sarkomerlänge entspricht. Sie erfassen Proportional- und Differentialänderungen, also Längenänderung und Beschleunigung derselben. Durch eine negative Rückkopplung, bei dem ein von der Muskelspindel ausgehendes Signal die Kontraktion des Muskels durch das UMN-Motoneuron mindert, schützen die Muskelspindeln weitgehend vor Überdehnung des Muskels. Daneben sind die Muskelspindeln für die Eigenreflexe verantwortlich, indem das von ihnen ausgesandte Signal auf dem gerade beschriebenen Wege zu einer Zuckung des Muskels beim Reflextest führt. Muskelspindeln sind 5-10 quergestreifte, mit einer Faszie umgebene Muskelfasern, beim Menschen meist 1-3 mm lang. Beim menschlichen Quadrizeps finden sich rund 500-1000 bis zu 10 mm lange Muskelspindeln. Die Anzahl der Muskelspindeln bestimmt darüber, wie fein die Kraftentfaltung eines Muskels dosiert werden kann. Die nicht-kontraktile Mitte der Muskelspindeln ist von afferenten sensiblen Fasern umsponnen, die auf eine Dehnung des Muskels mit einem Aktionspotential antworten, welches über den Spinalnerv in die graue Substanz des Hinterhorns und über eine Synapse an das alpha-Motoneuron geleitet wird. Die in den Regelkreislauf eingebettete Renshaw-Zelle bewirkt eine kurzfristige Hemmung der Kontraktion. Die kontraktilen Randbereiche der Muskelspindel besitzen eine gamma-Spindelschleife, die über motorische Nervenfasern mit den gamma-Motoneuronen verbunden sind und. Erzeugen die gamma-Spindelschleife ein Aktionspotential, führt das zu einer Kontraktion des Muskels, bei der der für eine Hemmung sorgende nicht-kontraktile mittlere Teil entspannt wird und sein Signal zurückfährt. Das geschieht in einer Regelschleife bis der mittlere Teil keine Dehnung mehr wahrnimmt. Die Spindeln sind mitverantwortlich dafür, daß der Muskel einen konstanten Tonus herstellt und beibehält, womit auch eine Gelenk in einer konstanten Position gehalten werden kann.
Hysterical Strength Pathway
Normalerweise stehen in Alltag und Sport immer nur ca. 35% der motorischen Einheiten gleichzeitig zur Verfügung. Wenn in Ausnahmesituationen die für die Gefahrenbewertung zuständige Amygdala eine existentielle Bedrohung detektiert, kann sie einen Impuls an den Hypothalamus aktivieren, der die Auswertung der Signale der Golgi-Sehenorganen ignorieren lässt und eine starke sympathische Reaktion und einen entsprechenden Adrenalin- und Cortisolausstoß auslöst, so daß eine gleichzeitige Kontraktion aller motorischen Einheiten möglich wird (Maximal Recruitment). Eine Ausschüttung von Endorphinen macht relativ unempfindlich gegen Schmerzempfindung. Mental herrscht eine extreme Fokussierung. Die resultierende totale Muskelkontraktion ist so stark, daß sie die eigenen Knochen brechen kann. Auch resultieren nicht selten Zerrungen oder Muskelrisse sowie Sehnenrisse. Außerdem ist danach eine zweite oder auch weitere ebenso intensive Kontraktionen nicht möglich. Daher wird diese Kapazität von Nervensystem normalerweise streng geschützt und ist auch durch gezieltes Training (Maximal Recruitment Training) nicht zu erreichen. Nach Beendigung der auslösenden Situation kehrt die Schmerzempfindung wieder auf normales Niveau zurück und es werden erlittene Schäden sowie deutliche Erschöpfung bei gleichzeitige hypercortisolärer Streßlage empfunden.
Schmerzanamnese (Kurzform)
– Lokalisation ? Ausdehnung ? Punktfömig, kreisförmig, flächig, länglich ? schmal, breit ? Richtung ?
– Qualität/Art (siehe unten) ? Veränderung ?
– Ruheschmerz / Bewegungsschmerz / Belastungsschmerz ?
– Zeitpunkt ? Dauer ? Erstauftreten ? mögliche Auslöser ?
– Stärke ? Verlauf ? Modalitäten (Einflußfaktoren) wie Tageszeit, Nahrungsaufnahme, Bewegung, andere ?
– Begleitsymptome ?
– Was verbessert, verschlechtert ?
– Muskulärer Schmerz oder nicht-muskulärer Schmerz ?
Schmerzqualitäten
Schmerzen können (ohne Anspruch auf Vollständigkeit) unterteilt werden:
1. sensorisch
-ausstrahlend
-bohrend
-brennend
-dumpf
-drückend
-dünn
-hell
-fein
-großflächig
-klopfend
-kolikartig
-krampfartig
-peitschend
-plötzlich (akut)
-pulssynchron
-reißend
-schleichend (ansteigend)
-schneidend
-stechend
-wehenartig
-wellenförmig
-klopfend
-pochend
-ziehend
-zuckend
-heiß
Beispiele:
stechend: Pleuritis
brennend: Hautabschürfung
ziehend: Rückenschmerzen
peitschend: Nervenschmerz, Gürtelrose
vernichtend: Herzinfarkt
bohrend: Tumore, auch Knochentumore
krampf/kolikartig: Nieren/Gallenkolik
wehenartig, krampfartig: Mensis
beklemmend: Angina pectoris
drückend: Schwellungen, Entzündungen
2. affektorisch (ohne Anspruch auf Vollständigkeit)
-beklemmend
-vernichtend
-heftig
-nervend
-lähmend
-schrecklich
-marternd
-quälend
Desweiteren können sie variieren, dies wird bezeichnet als:
Schmerzmodalitäten
Typische Schmerzmodalitäten sind etwa:
- Nacht/Tag
- Ruheschmerz /Bewegungsschmerz -Belastungsschmerz
- nach Aufregungen
- lageabhängig
- nach dem Essen/vor dem Essen (nüchtern)
- jahreszeitabhängig/ witterungsabhängig
- atemabhängig
- sich bessernd, verschlechternd
- Anlaufschmerz
Schmerzlokalitäten
Unabhängig vom von vielfältigen konkreten Orten (Lokalisation) können Ausdehnungen beschrieben werden, etwa:
punktuell
flächig
länglich oder quer ausgedehnt oder anderweitig ausgerichtet (Richtung ? Dicke ?)
oberflächlich (superfiziell) oder tief (profund, dann: wie tief?)
Charakteristische Schmerzen
Anlaufschmerz (Einlaufschmerz, Loslaufschmerz)
Schmerz, der zu Beginn einer Tätigkeit, Bewegung, Verrichtung auftritt und in ihrem weiteren Fortgang abklingt. Diese Art Schmerz ist typisch für Arthrose und Arthritis, aber auch andere degenerative Gelenkveränderungen, vor allem der Hüftgelenke und Kniegelenke. Im Falle der Arthrose verläuft die Erkrankung über die Jahre progredient, und somit wird aus dem anfänglichen Anlaufschmerz häufig ein durchgehender Belastungsschmerz und später auch Ruheschmerz. Bei der Arthrose sind beide insbesondere in arthritischen Schüben ausgeprägt.
Belastungsschmerz (stress induced pain)
der Schmerz, der durch Belastung belastungsschmerzhafter Teile des Bewegungsapparates ausgelöst wird.
Belastungsschmerzhaftigkeit
Die Eigenschaft eines Muskels, seiner Sehne oder einer anderen Struktur des Bewegungsapparates, Belastungsschmerz zu zeigen, also unter Belastung Schmerz zu zeigen, der eine andere Qualität hat als „Anstrengung“ oder „Dehnungsempfindung“, also anderen Ursprungs ist als aus den Propriozeptoren Golgi-Sehnenorgan oder Muskelspindel.
Die Last kann das eigene Körpergewicht sein oder ein externes Gewicht. Die Belastung durch das eigene Körpergewicht kann beispielsweise eine Kniebeuge, das Treppensteigen oder die notwendige Muskelarbeit für schnelles Gehen oder Laufen. Belastungsschmerzen betreffen hauptsächlich den Bewegungsapparat und haben ihre Ursache meist, aber nicht immer dort.
Bewegungsschmerz (pain in motion)
Schmerz, der unter aktiver oder passiver Bewegung ohne Belastung durch das Körpergewicht oder ein externes Gewicht auftreten. Der Bewegungsschmerz kann unterschieden werden in einen aktiven (die Bewegung wird vom Untersuchten selbst ausgeführt) und einen passiven unterschieden werden (die Bewegung wird von einem Untersucher ausgeführt). Bewegungsschmerzen sind typisch für spezielle Teile des Bewegungsapaprates wie Muskeln und Gelenke. Häufig sind Rücken, Schultergelenk und Kniegelenk betroffen. Die Ursachen für Bewegungsschmerzen können vielfältig sein: degenerative Erkrankungen des Bewegungsapparates, Frakturen, Rupturen, Fibromyalgie, Polyneuropathie, verschiedene Erkrankungen der WS oder auch Entzündungen.
Bewegungsschmerzhaftigkeit
Die Eigenschaft eines Teils des Bewegungsapparates (selten: innerer Organe) durch aktiv oder passiv verursachte Bewegung auch ohne Last Bewegungsschmerz auszulösen.
Dehnungsschmerz
Durch Dehnung, also Überführen eines Muskels in grenzwertig große oder immer größere Sarkomerlängen ausgelöste Schmerzempfindung, typischerweise ausstrahlend in Richtung des Muskelverlaufs lokalisierbar. Physiologischerweise ist Dehnungsschmerz von NRS 0 bis 10 skalierbar und klingt nach Ende der Krafteinwirkung auf den Muskel binnen Sekunden mit nur kurzem Nachhall deutlich ab. Die Propriozeptoren, die den Dehnungsschmerz melden, sind die Muskelspindeln.
Dehnungsschmerzhaftigkeit
Dehnungsschmerzhaftigkeit bezeichnet die Eigenschaft eines Teils des Bewegungsapparats (üblicherweise des Muskels und seiner Sehne) unter aktiv (durch Krafteinsatz der Antagonisten) oder passiv induzierter Dehnung des Muskels Schmerzhaftigkeit zu zeigen, die über das physiologische Maß an Dehnungsschmerzen hinausgeht oder eine andere Schmerzqualität zeigt. Verschiedene Erkrankungen des Muskels (z.B. Rupturen, Zerrungen, Muskelprellungen) oder der Sehne (z.B. Insertionstendopathien, Tendovaginitiden) können mit Dehnungsschmerzhaftigkeit verbunden sein.
Druckschmerz
Schmerz, der durch externe Intervention wie Palpation oder anderweitige mechanische Einwirkung auf ein Gewebe ausgelöst wird, welches Druckschmerzhaftigkeit (Druckdolenz) aufweist. Meist ist die Schmerzempfindung abhängig von der Intensität des Drucks. Bei diesem Druck kann es sich auch um durch Bekleidung oder Schuhwerk verursachten Druck handeln. Der Druckschmerz kann mit Stopp des externen Drucks sofort nachlassen oder ein wenig „nachhallen“ (Nachbelastungsschmerz). Druckschmerz weist sehr häufig auf eine Entzündung hin. Er muß begrifflich unterschieden werden von einem „drückenden Schmerz“, der eine erhöhte Spannung eines Gewebes anzeigt, ebenfalls häufig entzündlich bedingt ist, aber nicht durch willentlichen Druck von außen ausgelöst wird, sondern ohne irgendwelche Intervention gegeben ist.
Druckschmerzhaftigkeit / Druckdolenz
Druckschmerzhaftigkeit oder Druckdolenz bezeichnet die aktuelle Eigenschaft einer Körperstelle aktuell auf von außen ausgeübten Druck Schmerzempfindung (Druckschmerz) zu produzieren. Meist steht die Quantität der übermittelten Schmerzempfindung („Intensität“) mit der Höhe des ausgeübten Drucks in monotoner Abhängigkeit. Der resultierende Schmerz wird als Druckschmerz bezeichnet. Er darf nicht verwechselt werden mit dem Spannungsschmerz, der ohne externe Intervention wie Palpation auftritt.
funktioneller Schmerz
Funktioneller Schmerz ist kein scharf definierter Begriff. In der Regel werden darunter Schmerzen ohne nachweisbares nicht-klinisches Korrelat verstanden, das etwa im Nachweis einer Entzündung, eines Bruchs, einer Bursitis, eines Muskelfaserrisses, einer Arthrose oder anderen manifesten, nachweisbaren Störungen bestehen könnte. Häufig werden unter funktionellem Schmerz auch Schmerzen verstanden, die durch mit entsprechenden Mitteln durchaus nachweisbare, aber schwach auffällige Störungen entstehen, wie etwa die degenerativen Erscheinungen einer Insertionstendopathie. Zu den klassischen funktionalen Schmerzen gehören Muskelverspannungen, aber auch Veränderungen der Kapsel– oder Bandspannungen der Gelenke. Das begriffliche Gegenstück zum funktionellen Schmerz ist der strukturelle Schmerz.
ischämischer Schmerz (Ischämieschmerz, ischemic pain)
Ischämien sind vom Herzinfarkt bzw. der Vorstufe, der Angina Pectoris bekannt, treten aber auch an anderer Stelle auf, etwa als paVK in Form einer Claudicatio intermittens (Schaufensterkrankheit) auf, die schon mittlere Gehstrecken schmerzbedingt unmöglich macht. Auch die unblutige Apoplexie ist eine Ischämie, die allerdings zu keinem Schmerz führt (stumme Ischämie).
Klopfschmerz
Schmerzen die über das physiologische Maß hinaus durch Beklopfen einer anatomischen Struktur auftreten, etwa eine entzündete Stelle oder ein „kranker Zahn“.
Leistenschmerz
Funktioneller Schmerz oder struktureller Schmerz in der Leistenregion. Der funktionelle Schmerz wird in der Regel durch Insertionstendopathien folgender Muskeln verursacht:
Damit finden sich Muskeln aus verschiedenen Funktionalitäten, im wesentlichen: Bauchmuskeln, Hüftbeuger, Adduktoren. Der strukturelle Schmerz hingegen beruht auf manifesten strukturellen Störungen wie Gelenkblockaden (meist des ISG (ISG-Blockade), nachrangig des Hüftgelenks), Arthrose vor allem des Hüftgelenks (Coxarthrose), nachrangig des ISG, Störungen der Schambeinsymphyse, Frakturen und Stressfrakturen, bei Jüngeren auch Störungen des Hüftgelenks wie Morbus Perthes oder Morbus van Neck. Auch bei Erwachsenen finden sich nicht selten Störungsbilder, die auf in der Kindheit/Jugend unversorgte oder unzureichend versorgte Störungen dieser Art, auf Dysplasien und Inkongruenzen zurückgehen.
Die Sportanamnese ist bei Leistenschmerz häufig aufschlußreich und richtungsweisend. Häufig enstehen die Störungsbilder durch oder bei Fußball, Laufsportarten (insbesondere Sprint und Hürdenlauf), nachrangig beim Gehen, Springen und in Kampfsportarten. Bei akuten Verletzungen handelt es sich häufig um Muskelfaserrisse oder Sehnenrisse (bzw. Anrisse). Chronische Störungsbilder sind häufig Overuse-Syndrome, etwa Insertionstendopathien, Gelenkverschleiß (Arthrose) oft auf dem Boden kleiner Störungen des Bewegungsapparates wie Achsenfehlstellungen, Fußdeformitäten, muskulären Dysbalancen (z.B. Störungen oder Schwächen der Hüftmuskulatur). Bei der klinischen Untersuchung darf nicht übersehen werden, daß Angaben der Schmerzlokalistion nicht immer zuverlässig sind, da z.B. Störungen des Hüftgelenks in Richtung des Knies projizieren können oder des ISG in Richtung der Leiste.
Palpatorisch finden sich häufig eine diagnoseweisende Druckschmerzhaftigkeit. In Funktionstests (Seitenvergleich beachten!) können sich dehnungsschmerzhafte Bewegungseinschränkungen finden oder solche, die mit Gelenkschmerzen assoziiert sind. Gegen Widerstand ausgeführte Bewegungen zeigen durch Belastungsschmerzhaftigkeit meist Insertionstendopathien an, wenn der Schmerz insertionsnahe ist, sonst Störungen des Muskels selbst, was aber nicht in den Bereich des Störungsbildes Leistenschmerz fällt. Störung und Verminderung der Exorotation kann muskulär bedingt sein (Kontraktur/Verkürzung), aber auch bei entsprechender Schmerzangabe assoziiert mit Störungen des ISG. Einschränkungen der Endorotation hingegen sind in der Regel artikulärer Ursache und basieren auf Arthrose (meist Coxarthrose), Arthritis oder Kapsulitis. Sind die Bewegungen komplexer, bei denen Schmerzen oder Einschränkungen auftreten, muß weiter untersucht werden, oft findet sich die Ursache dann letztlich im Hüftgelenk. Beinlängendifferenzen sind immer (unter anderen verursachten Störungsbildern) auch Kandidaten für die Verursachung von Leistenschmerzen. Sind sie variabel (mal vorhanden, mal nicht), so geht dies oft eine Störung des ISG zurück.
Nachbelastungsschmerz (Schmerznachhall)
Klingt ein Belastungsschmerz nicht sofort nach Ende der Belastung ab, spricht man von einem Nachbelastungsschmerz, umgangssprachlich auch von einem „Nachhall“ des Schmerzes.
Nachtschmerz
Nachtschmerz bedeutet Schmerz, der nur nachts auftritt. Meist handelt es sich dabei um Gelenkschmerzen durch eine Arthritis, Arthrose sowie Erkrankungen des rheumatischen Formenkreises, insbesondere die rheumatoide Arthritis. Grundsätzlich treten Nachtschmerzen dieser Art häufig auch tags in (hinreichend langer) Ruhe auf. Im Rahmen der Schwangerschaft treten auch zuweilen Nachtschmerzen vor allem durch Flüssigkeitsansammlung in den Lymphgefäßen der Extremitäten (vor allem der Beine) auf. Dabei können mehrere Liter Flüssigkeit eingelagert werden, was zu Spannungsschmerzen und Druckschmerzhaftigkeit im Auflagebereich führt.
Pseudoradikulärer Schmerz
Unspezifische, örtlich begrenzte Schmerzen mit Ausstrahlung („übertragene Schmerzen“ oder „referred pain“) in Richtung einer Extremität ähnlich einer radikulären Schmerzsymptomatik, aber ohne deren efferente oder afferente neurologische Ausfälle (im Bereich Innvervation oder Sensitivität), da der Spinalnerv selbst in seiner Funktion nicht beeinträchtigt ist. Pseudoradikuläre Schmerzen treten z.B. als Folge eines Facettensyndroms, muskulärer oder gelenkiger Störungen, ISG-Blockaden auf.
pulssynchroner Schmerz (Pochen, Klopfen)
pulssynchroner Schmerz sind am weitesten verbreitet als Klopfen oder Pochen wie bei einem pochenden Kopfschmerz oder pochenden Zahnschmerzen. Auch Durafistelerkrankungen (pulssynchroner Tinnitus) weisen diese Charakteristik auf. Im Bewegungsapparat sidn pulsysynchrone Schmerzen seltener zu finden, hautsächlich im Zusammenhang mit Entzündungen, wenn die artierielle Versorgung pulssynchron zu Druckerhöhungen eines ohnehin gespanntens Gewebes führt.
Der Begriff klopfender Schmerz darf nicht mit Klopfschmerz, also dem Schmerz verwechselt werden, der mit dem Beklopfen einer klopfschmerzhaften Struktur ausgelöst wird.
Radikulärer Schmerz
Durch Reizung (z.B. durch Druck) einer Nervenwurzel hervorgerufener Schmerz, wie er bei einem Nervenwurzelkompressionssyndrom (Radikulopathie) auftritt. Ursächlich sind in der Regel Bandscheibengeschehen, Osteophyten oder Entzündungen. Typsicherweise projiziert der Schmerz in das Dermatom einer Nervenwurzel. Radiukläre Schmerzen sind abklärungsbedürftig und oft auch behandlungsbedürftig. Die Kompression von Nerven kann zu deren Atrophie führen, aber auch zu Atrophien der versorgten Muskulatur. Synonym wird auch die Bezeichnung neuroradikulär verwendet. Siehe den Unerschied zu pseudoradikulär hier.
Ruheschmerz
Schmerz, der (auch oder nur) in Ruhe auftritt ohne aktive oder passive Bewegung und ohne Belastung. Ruheschmerzhafte Körperteile sind meist auch bewegungsschmerzhaft. Ruheschmerz tritt im Bewegungsapparat häufig auf bei Arthrose, Arthritis, Insertionstendopathien, Frakturen, Nervenengpass-Syndromen (Karpaltunnelsyndrom, Kubilaltunnelsyndrom, Tarsaltunnelsyndrom), HWS-Syndrom. Weitere Arten von Ruheschmerz sind ischämische, kardiovaskuläre und neurologische Ruheschmerzen. Ruheschmerz kann von unterschiedlicher Qualität sein, etwa Spannungsschmerz (Entzündungen) oder bohrender Schmerz (Knochengeschehen).
Spannungsschmerz
Spannungsschmerz ist Schmerz, der duch eine erhöhte Gewebespannung in Geweben auftritt, die Rezeptoren bezitzen, um diese Art von Veränderung vom physiologischen Zustand zu registrieren und ans Gehirn zu übermitteln. Spannungsschmerz darf nicht mit Druckschmerzhaftigkeit (Druckdolenz) oder dem durch Palpation resultierenden Druckschmerz verwechselt werden. Ein klassisches Beispiel für deutlichen Spannungsschmerz mit zusätzlicher Druckschmerzhaftigkeit (Druckdolenz) ist Herpes labialis: bereits ohne Berührung besteht ein schmerzhaftes Spannungsempfinden, das durch Berührung oder Druck nochmals gesteigert werden kann. Die Schmerzqualität von Spannungsschmerz wird i.a. wie die bei Druckschmerz als „drückend“ oder „spannend“ bezeichnet.
Struktureller Schmerz
Struktureller Schmerz ist wie sein begriffliches Gegenteil, der funktionelle Schmerz, nicht hinreichend scharf definiert. Strukturelle Schmerzen sind solche, die durch eine (oft: nicht allzu aufwendig) nachweisbare Störung wie etwa eine Entzündung, einen Bruch, eine Burtisis, einen Muskelfaserriss, eine Arthrose entstehen.
Wachstumsschmerz
Wachstumsschmerzen sind beinbetonte nächtliche oder bereits abends beginnende Schmerzen, die meist bilateral auftreten, seltener auch in der oberen Extremität. Die sensorische Schmerzqualität wird meist als ziehend, brennend oder stechend beschrieben. Sie sind in der Regel harmlos und betreffen bis zu 30% der 3-12-Jährigen. Ätiologie und Pathogenese sind noch ungeklärt, Veränderungen des Blutbildes werden nicht beobachtet, hingegen eine familiäre Disposition.
Massagen, Kühlen, Massieren, Dehnen der lokalen Muskulatur werden zur Linderung empfohlen, bei Bedarf auch NSAR.
